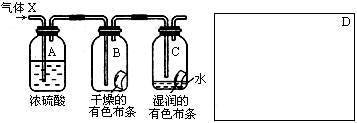题目内容
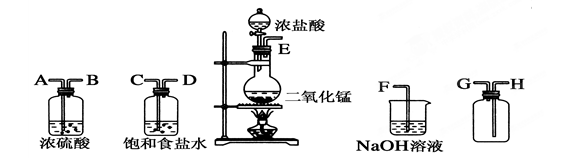
某化学小组用下列装置抽取收集纯净的氯气,并研究其性质。请回稳下列问题。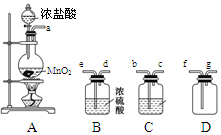
(1)装置A中发生反应的离子方程式为_______________________________。
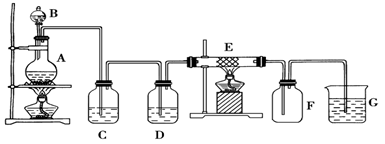
(2)按照气流方向各仪器接口的连接顺序为a→___________________→g。
(3)装置B中浓硫酸的作用是____________________________________________________________,装置C的试剂最好是___________________________________。
(4)某同学认为上述方案缺少尾气吸收装置,请在下面的方框中画出该装置并注明试剂。
| |
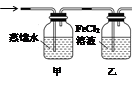
(5)装制取的氯气通入下图所示装置中,甲装置溶液中具有氧化性的含氯粒子是_______;如何证明乙装置中FeCl2溶液与Cl2发生了反应?(只回答需要的试剂和现象)___________________________。
(1)MnO2+4H++2Cl- Mn2++Cl2+2H2O(2分) (2)bcedf(2分)
Mn2++Cl2+2H2O(2分) (2)bcedf(2分)
(3)吸收水蒸气,干燥氯气(1分) 饱和食盐水(1分) (4) (2分)
(2分)
(5)Cl2、HClO、ClO-(2分) KSCN溶液(1分) 溶液变成红色(1分)
解析试题分析:(1)根据装置特点以及试剂可知,装置A是用来准备氯气的,所以A中发生反应的离子方程式为MnO2+4H++2Cl- Mn2++Cl2+2H2O。
Mn2++Cl2+2H2O。
(2)由于盐酸易挥发,所以生成的氯气中含有氯化氢以及水蒸气,因此在收集氯气之前需要首先除去氯化氢和水蒸气。首先除去的是氯化氢,所用试剂是饱和食盐水,然后在通过盛有浓硫酸的洗气瓶除去水蒸气。氯气的密度大于空气的,应该用向上排空气法收集,所以按照气流方向各仪器接口的连接顺序为a→b→c→e→d→f→g。
(3)根据以上分析可知,装置B中浓硫酸的作用是吸收水蒸气,干燥氯气;由于氯化氢极易溶于水,而氯气你溶于水,所以要除去氯气中的氯化氢气体最好选用饱和食盐水。
(4)氯气有毒,属于大气污染物,需要尾气处理。氯气能被氢氧化钠溶液吸收,所以可以用氢氧化钠溶液吸收,装置图为 。
。
(5)甲装置中盛有蒸馏水,氯气溶于水部分氯气与水反应生成盐酸和次氯酸,次氯酸是弱酸电离出氢离子和ClO-,所以甲装置溶液中具有氧化性的含氯粒子是Cl2、HClO、ClO-;氯气具有强氧化性,乙装置中盛有氯化亚铁溶液,能和氯气反应生成氯化铁。铁离子能和KSCN溶液反应而使溶液显红色,据此可以检验乙装置中FeCl2溶液与Cl2发生了反应。
考点:考查氯气制备、除杂、收集、尾气处理、性质以及铁离子的检验


 5CaCl2 + Ca(ClO3)2 + 6H2O
5CaCl2 + Ca(ClO3)2 + 6H2O

 = 。
= 。