题目内容
在氨水中存在下列电离平衡:NH3·H2O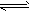 NH4++OH-,下列情况能引起电离平衡向正向移动的有
NH4++OH-,下列情况能引起电离平衡向正向移动的有
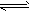 NH4++OH-,下列情况能引起电离平衡向正向移动的有
NH4++OH-,下列情况能引起电离平衡向正向移动的有[ ]
①加NH4Cl固体 ②加NaOH溶液 ③加HCl ④加CH3COOH溶液 ⑤加水 ⑥加压
A.①③⑤
B.①④⑥
C.③④⑤
D.①②④
A.①③⑤
B.①④⑥
C.③④⑤
D.①②④
C

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
题目内容
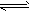 NH4++OH-,下列情况能引起电离平衡向正向移动的有
NH4++OH-,下列情况能引起电离平衡向正向移动的有
 阅读快车系列答案
阅读快车系列答案