题目内容
【题目】硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等。
(1)新制的绿矾(FeSO4·7H2O)是浅绿色的,但在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],写出该反应的化学方程式: 。
(2)已知FeSO4在不同条件下分解得到产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2;SO3熔点是16.8℃,沸点是44.8℃。
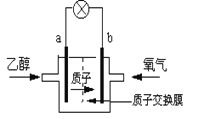
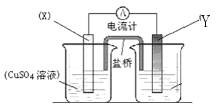
某研究性学习小组拟用下列装置进行实验探究“在加热条件下FeSO4的分解产物”。
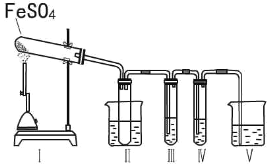
上述装置Ⅲ和Ⅳ用来检验气体产物。试回答下列问题:
①Ⅱ装置烧杯中水的温度应控制在 (选填“0℃、25℃、50℃”),装置Ⅱ的作用是 。
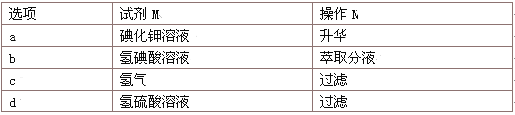
②装置Ⅲ中的试剂可以是 (选填序号,下同),现象是 ,则证明气体产物中含有SO3;装置Ⅳ中的试剂可以是 。
A.2mol/LNa2CO3溶液
B.品红溶液
C.0.5mol/L BaCl2溶液
D.0.5mol/LBa(NO3)2
E.0.01mol/L KMnO4溶液
F.淀粉碘化钾溶液
③装置V中试剂为NaOH溶液,发生反应的离子方程式为 。
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如下实验:
操作步骤 | 预期实验现象 | 预期实验结论 |
向其中一份溶液中加入 | 固体中含有Fe2O3 | |
向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液 | 产生蓝色沉淀 |
⑤若用22.8g FeSO4固体做实验,完全分解后,得到11.2g固体,其中Fe2O3的质量分数= (精确到0.1%)
【答案】(1)4FeSO4·7H2O + O2 = 4Fe(OH)SO4 +26H2O;
(2)①50℃,防止产生倒吸(或“用作安全瓶”)
②C,产生白色沉淀,B、E ;③SO2 +2OHˉ=SO32ˉ+H2O;
④
操作步骤 | 预期实验现象 | 预期实验结论 |
KSCN溶液(或硫氰化钾溶液) | 溶液变成血红色 | |
固体中含有FeO |
⑤35.7%。
【解析】
试题分析:(1)新制的绿矾(FeSO4·7H2O)在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],Fe2+被空气中的氧气氧化成Fe3+,则该反应的化学方程式是4FeSO4·7H2O + O2 = 4Fe(OH)SO4 +26H2O;
(2)①SO3的沸点是44.8℃,当温度高于44.8℃时三氧化硫为气体状态,把试管浸泡在50℃的热水浴中能防止SO3液化或凝固,产生的气体极易和溶液反应时,会产生倒吸,所以装置II的试管能防止溶液倒吸入装置Ⅰ中(或安全瓶),因此Ⅱ装置烧杯中水的温度应控制在50℃,装置Ⅱ的作用是防止产生倒吸(或“用作安全瓶”);
②装置III是检验是否有三氧化硫生成,可以选用氯化钡溶液,如果有白色沉淀生成说明有三氧化硫;装置IV是检验是否有二氧化硫,二氧化硫能使品红褪色,也能使酸性高锰酸钾溶液褪色,所以可以选用二者来检验二氧化硫;
③二氧化硫会污染空气,所以要用氢氧化钠溶液来吸收剩余的二氧化硫,其反应的离子方程式为:SO2 +2OHˉ=SO32ˉ+H2O;
④检验三价铁离子用硫氰化钾溶液,溶液变红色,证明有三价铁离子,进而说明固体产物中含有氧化铁;检验二价铁离子用K3 [Fe(CN)6 ]溶液,溶液中生成蓝色沉淀,说明有二价铁离子,即证明固体产物中含有FeO;
⑤反应过程中FeSO4固体分解为二氧化硫、三氧化硫、FeO、Fe2O3 ,完全分解后得到11.2g固体为氧化铁和氧化亚铁,质量减少的为二氧化硫和三氧化硫的总质量,设生成的二氧化硫为xmol,三氧化硫为ymol,根据硫元素守恒,则x+y=22.8g÷152g/mol=0.15mol,64x+80y=22.8g-11.2g=11.6g,解得:x=0.025,y=0.125,FeSO4固体分解,每生成1mol二氧化硫时硫元素得到2mol电子,每生成1mol Fe2O3时铁元素失去2mol电子,所以生成的二氧化硫与氧化铁的物质的量相同,则Fe2O3的物质的量为0.025mol,其质量为0.025mol×160g/mol=4.0g,质量分数为:(4.0g÷11.2g)×100%=35.7%。

 目标测试系列答案
目标测试系列答案【题目】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下面是八种短周期元素的相关信息(已知铍的原子半径为0.089 nm)
元素代号 | A | B | C | D | E |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
F原子中无中子,G最高正价数与负价数相等,且最外层电子数是次外层的二倍,H元素单质焰色反应呈黄色。
(1)C元素在元素周期表中的位置 。B形成的简单离子的结构示意图 。
(2)上述八种元素的最高价氧化物对应的水化物中酸性最强的是 (填化学式)。
(3)用电子式表示A、D形成化合物的过程: 。
(4)H、E形成原子个数比为1∶1的化合物中所含化学键类型为 。
(5)GE2的电子式为 ,F与G形成的最简单的化合物的结构式为 。
(6)E的氢化物比C的氢化物的熔沸点高的原因是 。
(7)A、B、C、E原子半径由大到小的顺序为(用元素符号表示) 。