题目内容
1. 为测定含有Na2O杂质的Na2O2样品的纯度,甲同学设计以下的方案.用如图所示装置,通过测定Na2O2与C02反应生成02的体积来测定样品的纯度.
为测定含有Na2O杂质的Na2O2样品的纯度,甲同学设计以下的方案.用如图所示装置,通过测定Na2O2与C02反应生成02的体积来测定样品的纯度.(1)C中所盛的药品是NaOH溶液
(2)A中橡皮管的作用是起恒压作用,使盐酸容易滴下;避免盐酸排空气使氧气体积偏大
(3)利用该实验方案所测Na2O2的纯度明显偏大,其原因可能是a、d (填选项字母).
a.装置A、B中的空气对测定结果产生了影响
b.装置C中的空气对测定结果产生了影响
c.读数时U形量气管中的液面左低右高
d.读数时U形量气管中的液面左高右低
(4)该法步骤相对麻烦,请设计一种简便的实验方法完成实验目的,画简图说明即可.
分析 通过测定Na2O2与C02反应生成02的体积来测定样品的纯度,装置图中稀盐酸滴入石灰石生成二氧化碳,进入装置B硬质玻璃管中反应,生成的氧气通过装置C中的氢氧化钠溶液除去剩余的二氧化碳气体,利用装置D量气管测定生成氧气体积,计算物质的量计算的过氧化钠的质量分数;
(1)氢氧化钠能和二氧化碳反应,不和氧气反应;
(2)橡皮管可以沟通锥形瓶和分液漏斗中的大气压强,还可以避免盐酸排空气;
(3)若果测的氧气的量比实际值高,则过氧化钠的纯度装置就会偏高,反之则偏低;
(4)称取一定质量样品,测定与水反应生成氧气的体积(标准状况),计算得到过氧化钠质量,得到样品的纯度;
解答 解:(1)C的作用是吸收二氧化碳,保证排水量气法获得的是氧气的体积,
故答案为:NaOH溶液;
(2)A中橡皮管可以沟通锥形瓶和分液漏斗,起恒压作用,使盐酸容易滴下,并且可以避免盐酸排空气使氧气体积偏大,
故答案为:起恒压作用,使盐酸容易滴下;避免盐酸排空气使氧气体积偏大;
(3)a、装置A、B中的空气会导致测得的氧气体积偏高,对测定结果产生影响,故a正确;
b、在调节U形量气管中的液面相平的过程中,排除了装置C中的空气对测定结果产生的影响,故b错误;
c、读数时U形量气管中的液面左低右高时,所测Na2O2的纯度会偏小,故c错误.
d、读数时U形量气管中的液面要保持向平,左高右低,所测Na2O2的纯度会偏大,故d正确;
故选ad.
(4)称取一定质量样品,测定与水反应,用量气管测定生成氧气的体积(标准状况),计算得到过氧化钠质量,得到样品的纯度,可以利用装置图测定;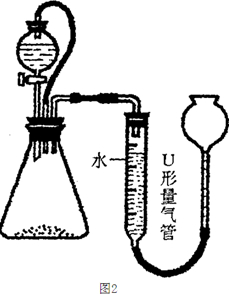 ;
;
故答案为: ;
;
点评 本题考查了物质纯度的实验设计和过程分析判断,主要是误差判断方法和装置设计应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
12.a、b、c、d、e、f、g为七种由短周期元素构成的微粒,它们都有10个电子,其结构特点如下:
其中b的离子半径大于e的离子半径;d是溶于水显碱性的四原子分子;c与f作用可生成2个中性分子g.
试写出:
(1)a微粒的原子结构示意图为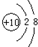
(2)b和e相应元素的最高价氧化物的水化物的碱性强弱比较为:NaOH>Mg(OH)2(用化学式表示).
(3)d的水溶液显碱性的原因(用电离方程式表示)NH3•H2O?NH4++OH-
(4)c微粒是OH-,f微粒是H3O+(用化学式表示).
(5)b相应的元素的单质与g微粒反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
| 微粒代码 | a | b | c | d | e | f | g |
| 原子核数目 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 带电荷数(单位电荷) | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
试写出:
(1)a微粒的原子结构示意图为
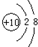
(2)b和e相应元素的最高价氧化物的水化物的碱性强弱比较为:NaOH>Mg(OH)2(用化学式表示).
(3)d的水溶液显碱性的原因(用电离方程式表示)NH3•H2O?NH4++OH-
(4)c微粒是OH-,f微粒是H3O+(用化学式表示).
(5)b相应的元素的单质与g微粒反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
9.在100mL混合酸的溶液中,硝酸的物质的量浓度为0.4mol/L,硫酸的物质的量浓度为0.2mol/L,向其中加入6.4g铜粉,微热,使其充分反应.生成NO的物质的量( )
| A. | 0.01mol | B. | 0.02mol | C. | 0.03mol | D. | 0.04mol |
6.据报道,${\;}_{67}^{166}$Ho可有效地治疗肝癌,该原子核内的中子数与核外电子数之差为( )
| A. | 32 | B. | 67 | C. | 99 | D. | 166 |
13.下列叙述正确的是( )
| A. | 甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色 | |
| B. | 有机物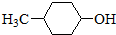 的消去产物有两种 的消去产物有两种 | |
| C. | 有机物C4H6O2能发生加聚反应,可推知其结构一定是CH2=CH-COOCH3 | |
| D. | 可用溴水鉴别苯酚、四氯化碳和乙酸 |
10.设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 常温下,含1 mol Fe的铁片与过量浓HNO3反应,转移电子的数目为3 NA个 | |
| B. | 19.2 g铜与足量的稀硝酸反应产生NO的体积为4.48 L | |
| C. | 标准状况下,33.6 L SO3含有9.03×1023个SO3分子 | |
| D. | 在46 gNO2和N2O4的混合物气体中所含原子总数为3NA个 |
9.工业上以锂辉石(Li2O•A12O3•4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂.其部分工艺流程如图1:

已知:①Li2O•Al2O3•4SiO2+H2SO4(浓)$\frac{\underline{\;250-300℃\;}}{\;}$Li2SO4+Al2O3•4SiO2•H2O↓
②不同温度下Li2CO3和Li2SO4的溶解度如下表:
(1)从滤渣1中分离出Al2O3的部分流程如下所示,括号中表示加入过量的试剂,方框表示所得到的物质.则步骤Ⅱ中反应的离子方程式是Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
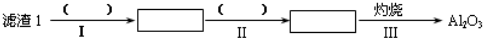
(2)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失.
(3)工业上用电解法将Li2CO3粗品制成高纯Li2CO3,其中向电解后所得的纯LiOH溶液中加入过量NH4HCO3溶液可生成Li2CO3,反应的化学方程式是2LiOH+NH4HCO3=Li2CO3↓+NH3+2H2O.

已知:①Li2O•Al2O3•4SiO2+H2SO4(浓)$\frac{\underline{\;250-300℃\;}}{\;}$Li2SO4+Al2O3•4SiO2•H2O↓
②不同温度下Li2CO3和Li2SO4的溶解度如下表:
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
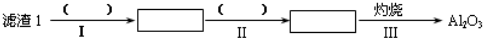
(2)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失.
(3)工业上用电解法将Li2CO3粗品制成高纯Li2CO3,其中向电解后所得的纯LiOH溶液中加入过量NH4HCO3溶液可生成Li2CO3,反应的化学方程式是2LiOH+NH4HCO3=Li2CO3↓+NH3+2H2O.

 .
.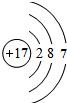 ,其最高价氧化物对应的水化物的化学式为HClO4.
,其最高价氧化物对应的水化物的化学式为HClO4.