��Ŀ����
����Ŀ��������ȩ�ǻ����л��ϳ�ԭ��֮һ��������ũҩ��ҽҩ����Ҫ�м��塣ij��ѧ��ȤС�������ͼ��ʾװ�ã��г֡����������ԣ���ģ�ҵ���������Ʊ�������ȩ��CCl3CHO����ʵ�顣
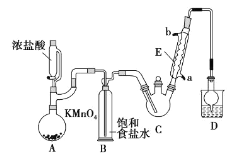
�������ϣ��й���Ϣ���£�
���Ʊ���Ӧԭ����C2H5OH+4Cl2��CCl3CHO+5HCl
���ܷ����ĸ���Ӧ��C2H5OH+HCl��C2H5Cl+H2O��CCl3CHO+HClO��CCl3COOH���������ᣩ+HCl
��������ʵ���Է��������������������ʣ�
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
��Է������� | 46 | 147.5 | 163.5 | 64.5 |
�۵�/�� | ��114.1 | ��57.5 | 58 | ��138.7 |
�е�/�� | 78.3 | 97.8 | 198 | 12.3 |
�ܽ��� | ��ˮ���� | ������ˮ���Ҵ� | ������ˮ���Ҵ���������ȩ | ����ˮ���������Ҵ� |
�ش��������⣺
(1)����E��������____������ˮ��������____�ڽ�ˮ������a������b������
(2)��ͬѧ��Ϊ��װ�ô���һ��ȱ�ݣ�Ӧ��BC֮���һ����װ�ã�������____��
(3)��װ��C���Ʒ�Ӧ�¶���70�����ң��ɲ���____���ȵķ�����
(4)װ��D����ܵ�����Ϊ____��װ��D�ձ��е��Լ���____��
(5)��Ӧ������C�еĻ�����з����Cl3CCOOH�ķ����ǣ������ƣ�____��
���𰸡����������� a ���ɵ������к���ˮ��������������ˮ��Ӧ����HCl��HClO���ᷢ������Ӧ������װ��C�и�����CCl3COOH��C2H5Cl���� ˮԡ ��ֹҺ�嵹�� ����������Һ ����
��������
Aװ�����ø��������Һ��Ũ�����Ʊ�������Bװ���ñ���ʳ��ˮ��ȥHCl��C�з�Ӧ�Ʊ�CCl3CHO��Dװ��ʢ������������Һ������β����������HCl��ֹ��Ⱦ�������ݴ˽��
(1)�������������֪E�����������ܣ�ˮ������Ӧ�����¿ڽ��Ͽڳ����ʴ�Ϊ�����������ܣ�a��
(2)�������ɵ������к���ˮ��������������ˮ��Ӧ����HCl��HClO���ᷢ������ӦCCl3CHO��HClO��CCl3COOH��HCl��C2H5OH��HCl��C2H5Cl��H2O������װ��C�и�����CCl3COOH��C2H5Cl���࣬��Ӧ��BC֮���һ����װ�ã��ʴ�Ϊ�����ɵ������к���ˮ��������������ˮ��Ӧ����HCl��HClO���ᷢ������Ӧ������װ��C�и�����CCl3COOH��C2H5Cl���ࣻ
(3)���Ʒ�Ӧ�¶���70 �����ң�Ӧ��ȡˮԡ���ȵķ������ʴ�Ϊ��ˮԡ��
(4)���������ų��������к����������Ȼ��⣬������Ҫ������������Һ���գ���ֹ��Ⱦ����������ܵ������Ƿ�ֹ�������ʴ�Ϊ����ֹҺ�嵹��������������Һ��
(5)CCl3COOH�����Ҵ���CCl3CHO��Ӧ��ȡ�������з��룬�ʴ�Ϊ������

 �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д� Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�����Ŀ��Ϊ��֤��ͬ���ϼ�����������ԭ�������������е��װ�ý���ʵ�顣
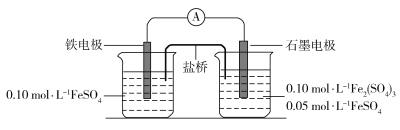
�ش��������⣺
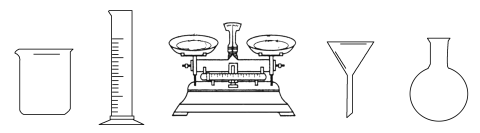
(1)��FeSO4��7H2O��������0.10 mol��L1 FeSO4��Һ����Ҫ��������ҩ�ס���������_________(������ͼ��ѡ��д������)��
(2)���װ���У������������缫�������Һ�����������������Ӳ�����Һ�е����ʷ�����ѧ��Ӧ�����ҵ�Ǩ����(u��)Ӧ�����ܵ�����������±����ݣ�������Ӧѡ��____________��Ϊ����ʡ�
������ | u����108/(m2��s1��V1) | ������ | u����108/(m2��s1��V1) |
Li+ | 4.07 |
| 4.61 |
Na+ | 5.19 |
| 7.40 |
Ca2+ | 6.59 | Cl | 7.91 |
K+ | 7.62 |
| 8.27 |
(3)��������ʾ���������缫����ʯī�缫����֪�������е������ӽ���________�缫��Һ�С�
(4)��ط�Ӧһ��ʱ�������缫��Һ��c(Fe2+)������0.02 mol��L1��ʯī�缫��δ��Fe��������֪��ʯī�缫��Һ��c(Fe2+)=________��
(5)����(3)��(4)ʵ��������֪ʯī�缫�ĵ缫��ӦʽΪ_______�����缫�ĵ缫��ӦʽΪ_______����ˣ���֤��Fe2+������С��________����ԭ��С��________��
(6)ʵ��ǰ��Ҫ�����缫��������FeSO4��Һ�м��뼸��Fe2(SO4)3��Һ�������缫����һ��ʱ�䣬���缫���汻��ʴ���������Ӧ��ɵķ�����_______��
����Ŀ����Ȫʵ��װ����ͼ��ʾ��Ӧ�����и�����������Һ���ܳ�����Ȫ�������
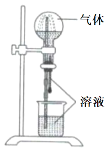
���� | ��Һ | |
A�� | H2S | ϡ���� |
B�� | HCl | ϡ��ˮ |
C�� | NO | ϡH2SO4 |
D�� | CO2 | ����NaHCO3��Һ |
A.AB.BC.CD.D
����Ŀ�����и��������У�������ͼ����һ��ת����ϵ��ѡ����
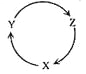
ѡ�� | X | Y | Z |
A | Na | NaOH | NaHCO3 |
B | Cu | CuSO4 | Cu(OH)2 |
C | C | CO | CO2 |
D | Si | SiO2 | H2SiO3 |
A.AB.BC.CD.D
