题目内容
某不纯的烧碱样品,含Na2CO3 3.8%(质量百分含量)、H2O 5.8%、NaHCO3 0.004%。取m g样品溶于40 m L 2 mol/L的盐酸后,并用2 mol/L Na OH溶液中和剩余的酸,在蒸发后可得干燥的固体的质量为( )
| A.4.68 g | B.5.58 g | C.2.34 g | D.3.34 g |
A
解析试题分析:完全反应后所得溶液的溶质为NaCl,根据Cl元素守恒,蒸发后所得NaCl的物质的量等于HCl的物质的量,所以m(NaCl)=0.04L×2mol/L×58.5g/mol=4.68g,故A项正确。
考点:本题考查化学计算。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关化学用语表示正确的是
A.N2的电子式: |
B.S2-的结构示意图: |
C.质子数为53,中子数为78的碘原子: |
| D.乙烯的分子式: CH2=CH2 |
在20℃时一刚性容器内部有一不漏气且可滑动的活塞将容器分隔成左、右室两室。左室充入N2,右室充入H2和O2,活塞正好停留离左端1/5处(如右图a)然后点燃引爆H2和O2混合器,活塞先左弹(设容器不漏气),恢复至原来温度,活塞恰好停在中间(如右图b),水蒸气的体积可忽略,则反应前H2和O2的体积比可能是( )
| A.1︰1 | B.1︰3 | C.7︰1 | D.5︰1 |
下列说法正确的是( )
| A.在标准状况下,1 mol水的体积是22.4 L |
| B.1 mol H2所占的体积约为22.4 L |
| C.在标准状况下, 阿伏加德罗常数个分子所占的体积约为22.4 L |
| D.在标准状况下,1 mol NH3和CO混合气体所占的体积约为22.4 L |
下列化学用语表达正确的是( )
| A.甲烷的标准燃烧热△H="-890.3" kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H="-890.3" kJ·mol-1 |
B.丙烯的键线式: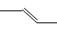 |
C.一定条件下,某密闭容器中充入2 mol SO2(g)和1 mol O2(g),达到平衡后,放出Q kJ热量,则该条件下的热化学方程式为:2SO2(g)+O2(g) 2SO3(g )△H=" -Q" kJ·mol-1 2SO3(g )△H=" -Q" kJ·mol-1 |
| D.乙烯的结构简式:CH2CH2 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A.含有NA个氦原子的氦气在标准状况下的体积约为11.2 L |
| B.25℃,1.01×105 Pa,32 g O2和O3的混合气体所含原子数为2.5NA |
| C.标准状况下,11.2 L H2O含有的原子数为1.5NA |
| D.常温常压下,44 g CO2含有的原子数为3NA |
下列说法正确的是
| A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L |
| B.从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol/L |
| C.配制500 mL 0.5 mol/L的CuSO4溶液,需62.5 g胆矾 |
| D.中和100 mL 1 mol/L的H2SO4溶液,需NaOH为4 g |
在相同温度和压强下,4个容器中分别装有4种气体,已知各容器中的气体和容器的容积分别是a.CO2,100 mL;b.O2,200 mL;c.N2,400 mL;d.CH4,600 mL,则4个容器中气体的质量由大到小的顺序是 ( )
| A.a>b>c>d | B.b>a>d>c | C.c>d>b>a | D.d>c>a>b |
用NA表示阿伏加德罗常数的值,下列说法错误的是
| A.23g Na变为Na+时失去的电子数为NA |
| B.32g O2中含有的分子数为2NA |
| C.在标准状况下22.4L H2中含有的氢分子数为NA |
| D.1 L0. 1 mol/LNa2CO3溶液中含有的钠离子数为0.2NA |