题目内容
在20℃时一刚性容器内部有一不漏气且可滑动的活塞将容器分隔成左、右室两室。左室充入N2,右室充入H2和O2,活塞正好停留离左端1/5处(如右图a)然后点燃引爆H2和O2混合器,活塞先左弹(设容器不漏气),恢复至原来温度,活塞恰好停在中间(如右图b),水蒸气的体积可忽略,则反应前H2和O2的体积比可能是( )
| A.1︰1 | B.1︰3 | C.7︰1 | D.5︰1 |
A
解析试题分析:左右压强相等,气体的物质的量之比等于体积之比,设氮气的物质的量为1mol,则H2和O2的物质的量为4mol,反应后活塞正好停留在容器的中间.说明反应后左右气体的物质的量相等,则右室内剩余气体1mol,反应的H2和O2共3mol,根据2H2+O2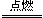 2H2O,可知反应的O2为1mol,反应的H2为2mol,若剩余的气体为H2,则反应前H2为3mol,O2为1mol,反应前H2和O2的体积比为3:1,若剩余的气体为o2,则反应前H2为2mol,O2为2mol,反应前H2和O2的体积比为1:1,故A项正确。
2H2O,可知反应的O2为1mol,反应的H2为2mol,若剩余的气体为H2,则反应前H2为3mol,O2为1mol,反应前H2和O2的体积比为3:1,若剩余的气体为o2,则反应前H2为2mol,O2为2mol,反应前H2和O2的体积比为1:1,故A项正确。
考点:本题考查过量计算。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案用密度1.19g/cm3质量分数为37%的浓盐酸配制稀盐酸:①用浓盐酸与等体积的水混合后所得稀盐酸的质量分数为a%②用浓盐酸与等质量的水混合后所得的稀盐酸的质量分数为b%,那么a与b的关系正确的是
| A.a>b | B.a="b" | C.a<b | D.无法确定 |
设阿伏伽德罗常数的值为NA,下列说法正确的是:
| A.0.5mol的NaHSO4固体中含有的阴离子总数为NA |
| B.0.1mol/L FeCl3的溶液中,含Cl-数目为0.3 NA |
| C.标准状况下22.4LNO2气体与水完全反应时,转移电子数目为NA |
| D.常温常压下,23gNO2和N2O4的混合气体中总原子数目为1.5 NA |
已知阿伏加德罗常数、物质的摩尔质量及1摩尔物质的体积,下列物理量中尚不能全部计算出其近似值的是( )
| A.气体物质分子的大小和质量 | B.液态物质分子的大小及质量 |
| C.固体物质分子的大小和质量 | D.气体物质分子的质量 |
科学家已发现一种新型氢分子,其化学式为H3。在相同条件下,等质量的H3和H2相同的是( )
| A.原子数 | B.分子数 | C.体积 | D.物质的量 |
在一定的温度、压强下,向100 mLCH4和Ar的混合气体中通入400 mL O2,点燃使其完全反应,最后在相同条件下得到干燥气体460 mL,则反应前混合气体中CH4和Ar的物质的量之比为 ( )
| A.1∶4 | B.1∶3 | C.1∶2 | D.1∶1 |
某不纯的烧碱样品,含Na2CO3 3.8%(质量百分含量)、H2O 5.8%、NaHCO3 0.004%。取m g样品溶于40 m L 2 mol/L的盐酸后,并用2 mol/L Na OH溶液中和剩余的酸,在蒸发后可得干燥的固体的质量为( )
| A.4.68 g | B.5.58 g | C.2.34 g | D.3.34 g |
下列说法正确的是(NA为阿伏加德罗常数)( )
| A.15g甲基(-CH3)所含有的电子数是NA |
| B.常温常压下,4g氦气所含有的原子数目为NA |
| C.标准状况下,1L己烷充分燃烧后生成的气态产物的分子数为6/22.4 NA |
| D.常温常压下,1mol乙烷所含有的共价键数目为8NA |