题目内容
为探究锌与稀盐酸反应速率[以v(H2)表示],向反应混合液中加入某些物质,下列判断正确的是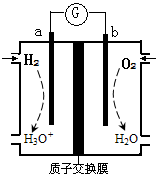
| A.加入铜粉,v(H2) 增大 |
| B.加入NaCl固体,会增大Cl—浓度,从而使v(H2)增大 |
| C.加入NaHSO4固体v(H2)不变 |
| D.加入水,锌不与水反应,v(H2)不变 |
A
解析试题分析:A、加入铜粉,锌和铜与稀盐酸构成原电池,使v(H2) 增大,正确;B、加入NaCl固体,虽然会增大Cl—浓度,但H+浓度基本不变,所以v(H2)基本不变,错误;C、加入NaHSO4固体后H+浓度增大v(H2)增大,错误;D、加入水,H+浓度减小,所以 v(H2)减小,错误。
考点:考查外界因素对化学反应速率的影响。

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
一定温度下,在体积一定的密闭容器中进行的可逆反应:C(s) + CO2(g)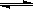 2CO(g),不能判断反应已经达到化学平衡状态的是
2CO(g),不能判断反应已经达到化学平衡状态的是
| A.v(CO2)= v(CO) | B.容器中总压强不变 |
| C.容器中混合气体的密度不变 | D.容器中CO的体积分数不变 |
在一不可变容器中发生如下反应:2NO2 2NO + O2 ΔH >0 达到平衡后,升温,混合气体的( )不变
2NO + O2 ΔH >0 达到平衡后,升温,混合气体的( )不变
| A.密度 | B.颜色 | C.压强 | D.总物质的量 |
运用相关化学知识进行判断,下列结论错误的是
| A.某吸热反应能自发进行,因此该反应是熵增反应 |
| B.NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 |
| C.可燃冰主要甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 |
| D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率 |
为探究锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入某些物质,下列判断正确的是
| A.加入NH4HSO4固体,v(H2)增大 | B.加入少量水,v(H2)不变 |
| C.加入CH3COONa固体,v(H2)减小 | D.滴加少量CuSO4溶液,v(H2)减小 |
在2L恒容密闭容器中充入2 mol X和lmol Y发生反应:2X(g)+Y(g) 3Z(g)△H<0, 反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g)△H<0, 反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
| A.升高温度,平衡常数增大 |
| B.W点X的正反应速率等于M点X的正反应速率 |
| C.Q点时,Y的转化率最大 |
| D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大 |
 设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是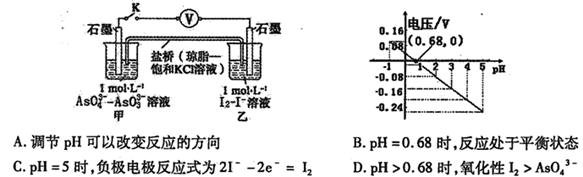
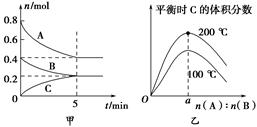
 zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是
zC(g)。图甲表示200 ℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是