题目内容
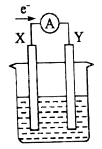
【题目】以N2和H2为反应物,盐酸酸化的NH4Cl溶液为电解质的原电池,工作原理如下图所示,下列说法不正确的是
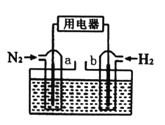
A. b电极为负极
B. 反应过程中,溶液中的Cl-向a电极移动
C. a电极的电极反应式为:N2+6e-+8H+=2NH4+
D. 电池反应为N2+3H2+2HCl=2NH4Cl
【答案】B
【解析】以N2和H2为反应物,盐酸酸化的NH4Cl溶液为电解质的原电池,该原电池的电池反应为:N2+3H2+2HCl=2NH4Cl。A项,通入N2的a电极为正极,通入H2的b电极为负极,正确;B项,反应过程中,Cl-向负极移动,向b电极移动,错误;C项,a电极上N2发生得电子的还原反应,电极反应式为N2+6e-+8H+=2NH4+,正确;D项,正确;答案选B。

练习册系列答案
相关题目