题目内容
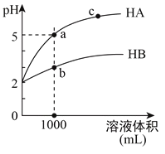
【题目】室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH随溶液体积的变化曲线如下图所示。下列说法正确的是
A.HA的酸性比HB的酸性弱
B.a点溶液的导电性比c点溶液的导电性强
C.若两溶液无限稀释,则它们的n(H+)相等
D.对a、b两点溶液同时升高温度,则![]() 增大
增大
【答案】B
【解析】
室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释至1000mL时,HA溶液PH=5,HB溶液PH<5,说明HA为强酸,HB为弱酸,据此分析解答。
室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释至1000mL时,HA溶液PH=5,HB溶液PH<5,说明HA为强酸,HB为弱酸,
A. 室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释至1000mL时,HA溶液PH=5,HB溶液PH<5,说明HA为强酸,HB为弱酸,A项错误;
B. a点溶液中离子浓度大于c点溶液中离子浓度,溶液导电性取决于离子浓度的大小,则a点溶液的导电性比c点溶液的导电性强,B项正确;
C. 溶液无限稀释接近为水的电离,氢离子浓度接近为10-7mol/L,若两溶液无限稀释,则它们的c(H+)相等,但是若体积不相等,则n(H+)不相等,C项错误;
D. HA为强酸,HB为弱酸,对a、b两点溶液同时升高温度,c(A-)浓度不变,HB电离程度增大,c(B-)浓度增大,则![]() 减小,D项错误;
减小,D项错误;
答案选B。

练习册系列答案
相关题目