题目内容
8.在A(g)+pB(g)?qC(g)的反应中,经t秒后C的浓度增加mmol.L-1,则用B浓度的变化来表示的反应速率是( )| A. | $\frac{pq}{mt}$mol/(L.S) | B. | $\frac{mt}{pq}$mol/(L.S) | C. | $\frac{mp}{qt}$mol/(L.S) | D. | $\frac{tp}{mq}$mol/(L.S) |
分析 根据v=$\frac{△c}{△t}$计算v(C),再利用速率之比等于化学计量数之比计算v(B).
解答 解:经t秒后C的浓度增加mmol.L-1,则v(C)=$\frac{mmol/L}{ts}$=$\frac{m}{t}$mol/(L.s),速率之比等于化学计量数之比,则v(B)=$\frac{p}{q}$则v(C)=$\frac{mp}{qt}$mol/(L.s),故选C.
点评 本题考查反应速率与化学计量数关系,比较基础,注意根据速率公式理解速率规律.

练习册系列答案
相关题目
18.某化学小组以苯甲酸(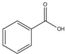 )为原料,制取苯甲酸甲酯.已知有关物质的沸点如下表:
)为原料,制取苯甲酸甲酯.已知有关物质的沸点如下表:
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2g苯甲酸(M=122g/mol)和20ml甲醇(密度约0.79g•mL-1 ),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品.
(1)若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式C6H5CO18OH+CH3OH$?_{△}^{浓H_{2}SO_{4}}$C6H5COOCH3+H218O;浓硫酸的作用是:催化剂、吸水剂.
(2)甲、乙、丙三位同学分别设计了如下图三套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).根据有机物的沸点,最好采用乙装置(填“甲”或“乙”或“丙”).
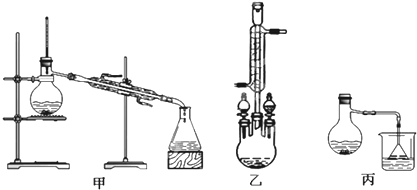
Ⅱ.粗产品的精制
(3)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程进行精制,请根据流程图写出操作方法的名称.操作Ⅰ分液 操作Ⅱ蒸馏.
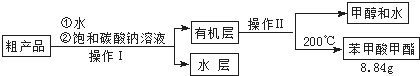
(4)能否用NaOH溶液代替饱和碳酸钠溶液?否(填“能”或“否”),并简述原因氢氧化钠是强碱,促进苯甲酸甲酯的水解,导致产品损失.
(5)通过计算,苯甲酸甲酯的产率是65%.
 )为原料,制取苯甲酸甲酯.已知有关物质的沸点如下表:
)为原料,制取苯甲酸甲酯.已知有关物质的沸点如下表:| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
在圆底烧瓶中加入12.2g苯甲酸(M=122g/mol)和20ml甲醇(密度约0.79g•mL-1 ),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品.
(1)若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式C6H5CO18OH+CH3OH$?_{△}^{浓H_{2}SO_{4}}$C6H5COOCH3+H218O;浓硫酸的作用是:催化剂、吸水剂.
(2)甲、乙、丙三位同学分别设计了如下图三套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).根据有机物的沸点,最好采用乙装置(填“甲”或“乙”或“丙”).

Ⅱ.粗产品的精制
(3)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程进行精制,请根据流程图写出操作方法的名称.操作Ⅰ分液 操作Ⅱ蒸馏.

(4)能否用NaOH溶液代替饱和碳酸钠溶液?否(填“能”或“否”),并简述原因氢氧化钠是强碱,促进苯甲酸甲酯的水解,导致产品损失.
(5)通过计算,苯甲酸甲酯的产率是65%.
16.下列叙述正确的是( )
| A. | 1 mol任何物质都含有NA个原子 | |
| B. | 硫酸的摩尔质量是98克 | |
| C. | 1 mol氮气的质量是28克 | |
| D. | 摩尔是国际单位制中七个基本物理量之一 |
3.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.已知实验室制备1,2-二溴乙烷可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚,温度过高时,乙醇又会被浓硫酸氧化.

有关数据列表如下:
回答下列问题:
(1)有关反应方程式是CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O和CH2=CH2+Br2→BrCH2CH2Br.
(2)在装置C中应加入c(填正确选项前的字母),其目的是吸收反应中可能生成的酸性气体
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备各反应已经结束的最简单方法是溴的颜色完全褪去;
(4)若产物中有少量副产物乙醚.可用蒸馏的方法除去;
(5)反应过程中应用冷水冷却装置D,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
(1)有关反应方程式是CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O和CH2=CH2+Br2→BrCH2CH2Br.
(2)在装置C中应加入c(填正确选项前的字母),其目的是吸收反应中可能生成的酸性气体
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备各反应已经结束的最简单方法是溴的颜色完全褪去;
(4)若产物中有少量副产物乙醚.可用蒸馏的方法除去;
(5)反应过程中应用冷水冷却装置D,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
17.下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是( )
①过滤 ②蒸发 ③向容量瓶转移液体.
①过滤 ②蒸发 ③向容量瓶转移液体.
| A. | ①和③ | B. | ①和② | C. | ②和③ | D. | ①②③ |
18.对于可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A. | 达到化学平衡时,4υ正(O2)=5υ逆(NO) | |
| B. | 若单位时间内生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态 | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | 化学反应速率关系是:2υ正(NH3)=3υ正(H2O) |
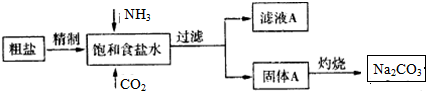
 某温度时,在一个5L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.试根据图中数据,填写下列空白:
某温度时,在一个5L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.试根据图中数据,填写下列空白: