题目内容
【题目】已知酸性: ![]() >H2CO3>
>H2CO3> ![]() ,将
,将 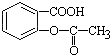 转变为
转变为 ![]() 的方法是( )
的方法是( )
A.与足量的NaOH溶液共热,再通入CO2
B.与稀H2SO4共热后,加入足量的NaOH溶液
C.加热溶液,通入足量的CO2
D.与稀H2SO4共热后,加入足量的NaHCO3溶液
【答案】AD
【解析】解:A.与足量的NaOH溶液共热,生成羧酸钠和酚钠结构,因 ![]() >H2CO3>
>H2CO3> ![]() ,则再通入足量的CO2生成邻羟基苯甲酸钠,故A正确;
,则再通入足量的CO2生成邻羟基苯甲酸钠,故A正确;
B.与稀H2SO4共热后,生成邻羟基苯甲酸,再加入足量的NaOH溶液,生成  ,故B错误;
,故B错误;
C.加热溶液,通入足量的CO2 , 不发生反应,故C错误;
D.与稀H2SO4共热后,生成邻羟基苯甲酸,加入足量的NaHCO3溶液,只有﹣COOH反应生成羧酸钠和酚结构,生成 ![]() ,故D正确;
,故D正确;
故选AD.
【考点精析】根据题目的已知条件,利用有机物的结构和性质的相关知识可以得到问题的答案,需要掌握有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解.

【题目】根据问题填空:
(1)已知H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJmol﹣1 . 若向三份等体积、等物质的量浓度的NaOH溶液中分别加入醋酸、浓硫酸、稀硝酸至恰好完全反应,并将上述过程中放出的热量分别记为Q1kJ、Q2kJ、Q3kJ.则三者的由小到大关系是(用Q1、Q2、Q3表示).
(2)如图所示A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其目的是; 若实验中不加盖泡沫塑料板,则求得的中和热数值(填偏大、偏小、无影响) 
(3)实验室用50mL 0.50molL﹣1盐酸、50mL 0.55molL﹣1NaOH溶液利用如图装置,进行测定中和热的实验.假设盐酸和氢氧化钠溶液的密度都是1g/cm3 , 又知中和后生成溶液的比热容c=4.18J/(g℃).为了计算中和热,实验时还需测量的数据有(填序号) .
A.反应前盐酸的温度
B.反应前盐酸的质量
C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.4 |
2 | 20.2 | 20.4 | 23.6 |
3 | 20.5 | 20.6 | 23.8 |
依据该学生的实验数据计算,该实验测得的中和热△H为 . (保留三位有效数字)



