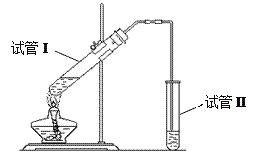
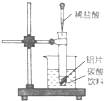
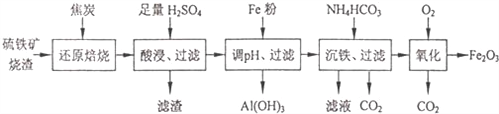
题目内容
【题目】如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是( )
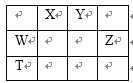
A. X、Y、Z三种元素最低价氢化物的沸点依次升高
B. 由X、Y和氢三种元素形成的化合物中只有共价键
C. 物质WY2、W3X4、WZ4均有熔点高、硬度大的特性
D. T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4
【答案】D
【解析】试题分析:W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22,则X、Y为第二周期元素,W、Z为第三周期元素,设X的最外层电子为x,则Y、W、Z的最外层电子数分别为x+1、x-1、x+2,所以x+x+1+x-1+x+2=22,解得x=5,即X为N,Y为O,W为Si,Z为Cl,W与T同主族,则T为Ge。A、X、Y、Z三种元素最低价氢化物分别为NH3、H2O、HCl,NH3、H2O中存在氢键,沸点都比HCl高,A项错误;B、N、H、O三种元素可形成NH4NO3,既有共价键也有离子键,B项错误;C、SiO2、Si3N4属于原子晶体,熔点高,硬度大,而SiCl4属于分子晶体,熔点低,硬度小,C项错误;D、Ge元素位于金属与非金属之间的分界线,因此具有半导体的特性,与碳属于同一主族,最外层四个电子,性质相似,可形成GeCl4,D项正确;答案选D。

【题目】某化学小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备NiSO47H2O.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).
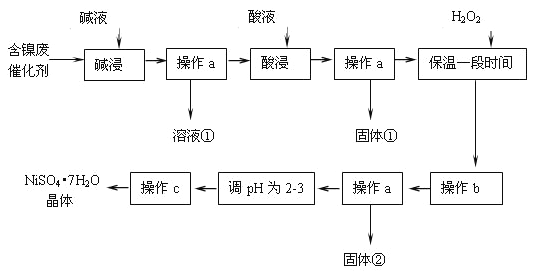
部分阳离子以氢氧化物形式沉淀时的pH如下:
沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
Al(OH)3 | 3.8 | 5.2 |
Fe(OH)3 | 2.7 | 3.2 |
Fe(OH)2 | 7.6 | 9.7 |
Ni(OH)2 | 7.1 | 9.2 |
(1)操作a应选用下列哪种方法或装置:_____
A.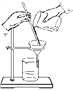 B.
B. C.
C.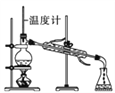 D.
D.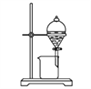
(2)“碱浸”过程中发生反应的离子方程式是________
(3)“酸浸”时所加入的酸是________(填化学式).
(4)加入H2O2时发生反应的离子方程式为________
(5)操作b为调节溶液的pH,你认为pH的调控范围是________
(6)产品晶体中有时会混有少量绿矾(FeSO47H2O),其原因可能是____(写出一点即可).
(7)NiSO47H2O可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M=NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为________.
【题目】A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
元素 | 相关信息 |
A | 原子核外有6种不同运动状态的电子 |
C | 基态原子中s电子总数与p电子总数相等 |
D | 原子半径在同周期元素中最大 |
E | 基态原子价层电子排布式为3s23p1 |
F | 基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反 |
G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
H | 是我国使用最早的合金中的最主要元素 |
请用化学用语填空:
(1)A元素在元素周期表中的位置______,B元素和C元素的第一电离能比较,较大的是___________,C元素和F元素的电负性比较,较小的是_____________。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为____________,B元素所形成的单质分子中![]() 键与π数目之比为_________。
键与π数目之比为_________。
(3)G元素的低价阳离子的结构示意图是_________________,F元素原子的价电子排布图是__________,H元素的基态原子核外电子排布式是________________________________________。
(4)G的高价阳离子的溶液与H单质反应的离子方程式为_____________________________;与E元素成对角关系的某元素的最高价氧化物对应的水化物具有两性,该两性物质与D元素的最高价氧化物对应的水化物反应的化学方程式为________________________________。