题目内容
短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示:
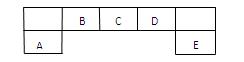
请回答下列问题:
 (1)B、C、D元素电负性的大小顺序为:______>______>______(填元素符号)。
(1)B、C、D元素电负性的大小顺序为:______>______>______(填元素符号)。
 (2)E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为_______________________________________________.
(2)E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为_______________________________________________.
 (3)C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L甲气体与0.5L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是__________.
(3)C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L甲气体与0.5L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是__________.
 (4)在298K下,A、B的单质各1mol完全燃烧,分别放出热量a kJ和b kJ。又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来,若此置换反应生成3molB的单质,则该反应在298K下的
(4)在298K下,A、B的单质各1mol完全燃烧,分别放出热量a kJ和b kJ。又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来,若此置换反应生成3molB的单质,则该反应在298K下的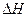 = (注:题中所设单质均为最稳定单质)
= (注:题中所设单质均为最稳定单质)
 (5)要证明与D同主族相邻元素F的非金属性与E的非金属性的强弱,正确、合理的实验操作及现象是
(5)要证明与D同主族相邻元素F的非金属性与E的非金属性的强弱,正确、合理的实验操作及现象是
(6)用A、B的单质作电极,C的最高价氧化物的水化物稀溶液作电解质溶液构成原电池,写出此原电池正极的电极反应式 。(假设C只被还原至+2价)

请回答下列问题:
 (1)B、C、D元素电负性的大小顺序为:______>______>______(填元素符号)。
(1)B、C、D元素电负性的大小顺序为:______>______>______(填元素符号)。 (2)E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为_______________________________________________.
(2)E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为_______________________________________________. (3)C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L甲气体与0.5L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是__________.
(3)C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L甲气体与0.5L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是__________. (4)在298K下,A、B的单质各1mol完全燃烧,分别放出热量a kJ和b kJ。又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来,若此置换反应生成3molB的单质,则该反应在298K下的
(4)在298K下,A、B的单质各1mol完全燃烧,分别放出热量a kJ和b kJ。又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来,若此置换反应生成3molB的单质,则该反应在298K下的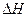 = (注:题中所设单质均为最稳定单质)
= (注:题中所设单质均为最稳定单质) (5)要证明与D同主族相邻元素F的非金属性与E的非金属性的强弱,正确、合理的实验操作及现象是
(5)要证明与D同主族相邻元素F的非金属性与E的非金属性的强弱,正确、合理的实验操作及现象是 (6)用A、B的单质作电极,C的最高价氧化物的水化物稀溶液作电解质溶液构成原电池,写出此原电池正极的电极反应式 。(假设C只被还原至+2价)
 (1)O>N>C(2分)
(1)O>N>C(2分) (2)8HCl+KClO4
(2)8HCl+KClO4 KCl+4Cl2↑+ 4H2O(3分)
KCl+4Cl2↑+ 4H2O(3分)(3) NaNO2(2分)
 (4)
(4) -(4a–3b)KJ/mol或(3b–4a)KJ/mol(3分)
-(4a–3b)KJ/mol或(3b–4a)KJ/mol(3分) (5) 将氯水(或氯气)滴入(通入)到硫化钠(或硫化氢等)溶液中,有淡黄色沉淀生成。(其他合理答案亦可)(2分)
(5) 将氯水(或氯气)滴入(通入)到硫化钠(或硫化氢等)溶液中,有淡黄色沉淀生成。(其他合理答案亦可)(2分)(6)NO3-+3e-+4H+=NO↑+2H2O(2分)
A、B、C、D、E五种元素分别是Al、C、N、O、Cl, (1)
(1) 电负性O>N>C;(2)
电负性O>N>C;(2)
 生成的气体单质是Cl2,反应的化学方程式为:8HCl+KClO4
生成的气体单质是Cl2,反应的化学方程式为:8HCl+KClO4 KCl+4Cl2↑+ 4H2O;(3)
KCl+4Cl2↑+ 4H2O;(3) 氮的氧化物中,NO相对分子质量最小,2L NO与0.5LO2混合后先生成1L NO与1L NO2的混合气体,再与NaOH溶液发生下列反应:NO+NO2+2NaOH =2NaNO2+H2O,所以生成的盐是NaNO2;(也可用电子守恒法推出N在盐中显+3价,所以是NaNO2。)(4)
氮的氧化物中,NO相对分子质量最小,2L NO与0.5LO2混合后先生成1L NO与1L NO2的混合气体,再与NaOH溶液发生下列反应:NO+NO2+2NaOH =2NaNO2+H2O,所以生成的盐是NaNO2;(也可用电子守恒法推出N在盐中显+3价,所以是NaNO2。)(4)
 在298K下,1molAl(s)完全燃烧放出热量aKJ,1molC(s)完全燃烧放出热量bKJ,根据盖斯定律,可得:-(4a–3b)KJ/mol或(3b–4a)KJ/mol;(5)
在298K下,1molAl(s)完全燃烧放出热量aKJ,1molC(s)完全燃烧放出热量bKJ,根据盖斯定律,可得:-(4a–3b)KJ/mol或(3b–4a)KJ/mol;(5)
 要证明S的非金属性与Cl的非金属性强弱,可以利用置换反应,将氯水(或氯气)滴入到硫化钠(或硫化氢等)溶液中即可(其他答案:如分别将硫化氢、HCl加热,硫化氢分解生成淡黄色固体而HCl不分解或比较高氯酸与硫酸的酸性,高氯酸的酸性强等较合理答案可给1分)。
要证明S的非金属性与Cl的非金属性强弱,可以利用置换反应,将氯水(或氯气)滴入到硫化钠(或硫化氢等)溶液中即可(其他答案:如分别将硫化氢、HCl加热,硫化氢分解生成淡黄色固体而HCl不分解或比较高氯酸与硫酸的酸性,高氯酸的酸性强等较合理答案可给1分)。
 (1)
(1) 电负性O>N>C;(2)
电负性O>N>C;(2)
 生成的气体单质是Cl2,反应的化学方程式为:8HCl+KClO4
生成的气体单质是Cl2,反应的化学方程式为:8HCl+KClO4 KCl+4Cl2↑+ 4H2O;(3)
KCl+4Cl2↑+ 4H2O;(3) 氮的氧化物中,NO相对分子质量最小,2L NO与0.5LO2混合后先生成1L NO与1L NO2的混合气体,再与NaOH溶液发生下列反应:NO+NO2+2NaOH =2NaNO2+H2O,所以生成的盐是NaNO2;(也可用电子守恒法推出N在盐中显+3价,所以是NaNO2。)(4)
氮的氧化物中,NO相对分子质量最小,2L NO与0.5LO2混合后先生成1L NO与1L NO2的混合气体,再与NaOH溶液发生下列反应:NO+NO2+2NaOH =2NaNO2+H2O,所以生成的盐是NaNO2;(也可用电子守恒法推出N在盐中显+3价,所以是NaNO2。)(4)
 在298K下,1molAl(s)完全燃烧放出热量aKJ,1molC(s)完全燃烧放出热量bKJ,根据盖斯定律,可得:-(4a–3b)KJ/mol或(3b–4a)KJ/mol;(5)
在298K下,1molAl(s)完全燃烧放出热量aKJ,1molC(s)完全燃烧放出热量bKJ,根据盖斯定律,可得:-(4a–3b)KJ/mol或(3b–4a)KJ/mol;(5)
 要证明S的非金属性与Cl的非金属性强弱,可以利用置换反应,将氯水(或氯气)滴入到硫化钠(或硫化氢等)溶液中即可(其他答案:如分别将硫化氢、HCl加热,硫化氢分解生成淡黄色固体而HCl不分解或比较高氯酸与硫酸的酸性,高氯酸的酸性强等较合理答案可给1分)。
要证明S的非金属性与Cl的非金属性强弱,可以利用置换反应,将氯水(或氯气)滴入到硫化钠(或硫化氢等)溶液中即可(其他答案:如分别将硫化氢、HCl加热,硫化氢分解生成淡黄色固体而HCl不分解或比较高氯酸与硫酸的酸性,高氯酸的酸性强等较合理答案可给1分)。
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 13分)下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
13分)下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题: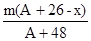 mol
mol mol
mol  mol
mol mol
mol
 ___,其中的化学键类型为:______________。
___,其中的化学键类型为:______________。