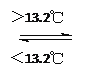题目内容
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g),反应进行到10 s末达到平衡,此时测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+2D(g),反应进行到10 s末达到平衡,此时测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________。
(2)10 s末,生成物D的浓度为________。
(3)A与B的平衡转化率之比为________。
(4)反应过程中容器内气体的平均相对分子质量变化是_____(填“增大”、“减小”或“不变”,下同),气体的密度变化是______。
(5)在一定温度下,体积不变的密闭容器中,上述反应达到平衡的标志是_______(填字母)。
A. 气体总质量保持不变 B. A、B、C、D的浓度都相等
C. 每消耗3 mol A的同时生成2 mol D D. A、B、C、D的分子数之比为3∶1∶2∶2
E. 3V正(A) = 2V逆(C) F. A的转化率保持不变
【答案】0.04 mol·L-1·s-1 0.4 mol·L-1 1∶1 不变 不变 F
【解析】
(1)依据化学反应速率的基本定义式作答;
(2)依据生成D的物质的量进行计算;
(3)依据转化率的定义结合题意分析作答;
(4)混合气体的质量和物质的量、容器的体积均不变化;
(5)根据平衡状态判断的标志作答;
(1)![]() =
=![]() =0.04 mol·L-1·s-1;
=0.04 mol·L-1·s-1;
(2)根据方程式可知,10s末,生成物D的物质的量与C的物质的量相等,为0.8mol,则10s末,生成物D的浓度为![]() = =0.4mol/L;
= =0.4mol/L;
(3)平衡转化率等于转化量与初始量的比值,因平衡时A与B的物质的量之比等于1.8mol:0.6mol=3:1,转化量之比等于化学计量数之比也等于3:1,则平衡转化率之比:![]() =1:1;
=1:1;
(4)反应过程中容器内气体的总质量保持不变,总的物质的量保持不变,则平均相对分子质量不变,又是在固定容积为2 L的密闭容器中进行,则气体的体积保持不变,即气体的密度不变;
(5)由反应3A(g)+B(g)![]() 2C(g)+2D(g)可知:
2C(g)+2D(g)可知:
A.气体总质量始终保持不变,不能说明反应达到平衡状态,A项错误;
B. A、B、C、D的浓度都相等,不能说明浓度保持不变,则不能说明反应达到平衡状态,B项错误;
C. 每消耗3 mol A的同时生成2 mol D,均表示的正反应方向,C项错误;
D.A、B、C、D的分子数之比为3∶1∶2∶2,不能说明反应的物质的量保持不变,D项错误;
E. 2V正(A) =3 V逆(C),说明正反应速率等于逆反应速率,反应已经达到平衡状态,但题中的定量关系不能说明反应达到平衡状态,E项错误;
F. A的转化率保持不变,说明反应达到平衡状态,F项正确;
答案选F。

 阅读快车系列答案
阅读快车系列答案