题目内容
【题目】用可再生的物质制备乙酸乙酯的绿色合成路线之一如图所示:

⑴M的化学式为_______________________;
⑵反应③的反应类型为____________________;
⑶写出反应④的化学方程式: _____________________________;
⑷写出反应②的方程式: ______________________________。
【答案】C6H12O6 氧化反应 CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O C6H12O6
CH3COOCH2CH3+H2O C6H12O6 ![]() 2 CH3CH2OH+2CO2↑
2 CH3CH2OH+2CO2↑
【解析】
淀粉或纤维素完全水解得到葡萄糖,葡萄糖经酒化酶的作用生成乙醇;乙醇可以被酸性高锰酸钾氧化生成乙酸,乙酸和乙醇发生酯化反应生成乙酸乙酯。
(1)M为葡萄糖,化学式为C6H12O6;
(2)乙醇到乙酸,增加了氧原子减少了氢原子,所以为氧化反应;
(3)该反应为乙酸和乙醇的酯化反应,方程式为CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(4)反应②为葡萄糖在酶的作用下生成乙醇和二氧化碳,方程式为C6H12O6 ![]() 2 CH3CH2OH+2CO2↑。
2 CH3CH2OH+2CO2↑。

【题目】反应X(g)![]() 4Y(g)+Z(g),在200℃和T℃时,X 的物质的量浓度(单位:mol·L-1)随时间变 化的有关实验数据见下表:
4Y(g)+Z(g),在200℃和T℃时,X 的物质的量浓度(单位:mol·L-1)随时间变 化的有关实验数据见下表:
时间/min | 0 | 2 | 4 | 6 | 8 | 10 |
200/℃ | 0.80 | 0.55 | 0.35 | 0.20 | 0.15 | 0.15 |
T/℃ | 1.00 | 0.65 | 0.35 | 0.18 | 0.18 | 0.18 |
下列有关该反应的描述正确的是
A. 在200℃时,4min内用Y表示的化学反应速率为0.1125mol·L-1·min-1
B. T℃下,6min时反应刚好达到平衡状态
C. 根据上表内 X 的浓度变化,可知浓度越大,反应速率越大
D. 从表中可以看出T <200
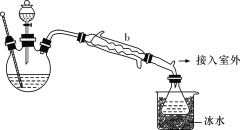
【题目】利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。
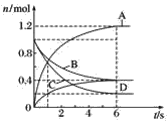
(1)T1℃时,在2L密闭容器中充入0.6molSO3,图1表示SO3物质的量随时间的变化曲线。

①平衡时,SO3的转化率为______(保留一位小数);在T1℃下反应2SO2(g)+O2(g) ![]() 2SO3(g) 的平衡常数为____________;若其他条件不变,在8min时压缩容器的体积至1L,则n(SO3)的变化曲线为_______(填字母)。
2SO3(g) 的平衡常数为____________;若其他条件不变,在8min时压缩容器的体积至1L,则n(SO3)的变化曲线为_______(填字母)。
②下表为不同温度(T)下反应2SO2(g)+O2(g) ![]() 2SO3(g) △H<0的化学平衡常数(K):
2SO3(g) △H<0的化学平衡常数(K):
T/℃ | T2 | T3 |
K | 20.5 | 4.68 |
由此推知,其他条件相同,在T1、T2、T3三种不同温度下,反应从开始至达到平衡时所需要的时间最长的是 _____________。(填“T1”、“T2”或“T3”)
(2)在体系恒压的条件下进行反应:2SO2(g)+O2(g) ![]() 2SO3(g),原料气中SO2和O2的物质的量之比(k)不同时,SO2的平衡转化率与温度(t)的关系如图2所示:图中k1、k2、k3的大小顺序为____________。
2SO3(g),原料气中SO2和O2的物质的量之比(k)不同时,SO2的平衡转化率与温度(t)的关系如图2所示:图中k1、k2、k3的大小顺序为____________。

【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
B. 红棕色气体不能表明②中木炭与浓硝酸产生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
【题目】下列粒子![]() 分子或离子
分子或离子![]() 均含有18个电子:
均含有18个电子:
粒子 | A+ | B2- | C | D | E | F |
组成特点 | 单核离 | 化合物, 双核分子 | 单质, 双核分子 | 化合物, 三核分子 | 化合物, 四核分子 | |
下列说法错误的是
A.A的元素符号是K,B2-的离子结构示意图是![]()
B.C的浓溶液可用于实验室制Cl2
C.D的单质具有强氧化性,可将其同族元素的单质从盐溶液中置换出来
D.F中可能既含极性键又含非极性键