题目内容
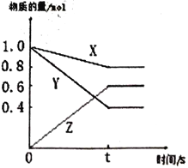
【题目】某温度下,气体X和Y在体积为2L的密闭容器中反应,生成气体Z。经测定各物质的物质的量随时间变化如下图所示,经10s达到化学平衡状态,请回答下列问题。
(1)写出该反应的化学反应方程式____________________________________。
(2)0-10s内,Y的平均反应速率为______________________。
(3)达到平衡时,X的转化率为______________________。
【答案】 X+3Y![]() 3Z 0.03mol·L-1·s-1 20%
3Z 0.03mol·L-1·s-1 20%
【解析】根据图像可知X与Y的起始量均是1mol,达到平衡后X是0.8mol,Y是0.4mol,说明X与Y是反应物,Z是生成物,结合图像分析解答。
(1)达到平衡后X减少了1mol-0.8mol=0.2mol,Y减少了1mol-0.4mol=0.6mol,Z增加了0.6mol,因此根据变化量之比是化学计量数之比可知X、Y、Z的化学计量数之比是0.2:0.6:0.6=1:3:3,则该反应的化学反应方程式为X+3Y![]() 3Z;
3Z;
(2)0~10s内Y浓度的变化量是0.6mol÷2L=0.3mol/L,则Y的平均反应速率为0.3mol/L÷10s=0.03mol·L-1·s-1;
(3)达到平衡时,X的转化率为0.2mol/1mol×100%=20%。

练习册系列答案
相关题目