题目内容
17.用氯气给自来水消毒,某学生用自来水配制下列物质的溶液,药品不会产生明显变质的是( )| A. | 石蕊 | B. | 硝酸银 | C. | 亚硫酸钠 | D. | 氯化铝 |
分析 用氯气给自来水消毒,发生反应Cl2+H2O?HCl+HClO,溶液中存在的微粒有Cl2、HClO、HCl、Cl-、H+、H2O,氯气和次氯酸具有强氧化性,溶液呈酸性,氯离子能和银离子反应生成AgCl沉淀,据此分析解答.
解答 解:用氯气给自来水消毒,发生反应Cl2+H2O=HCl+HClO,溶液中存在的微粒有Cl2、HClO、HCl、Cl-、H+、H2O,
A.溶液呈酸性,酸能使石蕊变色,所以不能用自来水配制石蕊,故A不选;
B.溶液中含有氯离子,氯离子和银离子反应生成AgCl白色沉淀,所以不能用自来水配制硝酸银溶液,故B不选;
C.氯气、次氯酸都具有强氧化性,能氧化亚硫酸钠生成硫酸钠,所以不能用自来水配制亚硫酸钠溶液,故C不选;
D.氯化铝属于强酸弱碱盐,和氯气、次氯酸、盐酸等都不反应,所以可以用自来水配制氯化铝溶液,故D选;
故选D.
点评 本题以氯气为载体考查氯水性质,明确氯水中成分及各微粒性质是解本题关键,注意氯气、次氯酸的强氧化性,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.天然铊有两种稳定同位素,${\;}_{81}^{203}$Tl和${\;}_{81}^{205}$Tl.下列有关铊的同位素说法中,不正确的是( )
| A. | ${\;}_{81}^{203}$Tl和${\;}_{81}^{205}$Tl质子数相同 | |
| B. | ${\;}_{81}^{203}$Tl和${\;}_{81}^{205}$Tl互为同素异形体 | |
| C. | ${\;}_{81}^{203}$Tl和${\;}_{81}^{205}$Tl中子数之差为2 | |
| D. | ${\;}_{81}^{205}$Tl原子核内中子数与核外电子数之差为43 |
5.下列说法正确的是( )
| A. | 乙酸和乙醇都属烃类化合物 | |
| B. | 有机化合物一定含有碳元素 | |
| C. | 丙烷和丁烷都有同分异构体 | |
| D. | 燃烧生成CO2和H2O的物质不一定是烃类 |
12.氢气还原氧化铜:CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$H2O+Cu,在该反应说法不正确的是( )
| A. | H2做还原剂 | B. | CuO做氧化剂 | ||
| C. | 铜元素的化合价降低 | D. | 铜元素化合剂升高 |
2.将湿润的红色石蕊试纸放在进行下列实验的试管口,试纸变蓝色的有( )
| A. | 加热浓氨水 | B. | 加热NH4Cl固体 | ||
| C. | 加热NH4Cl和Ca(OH)2的混合物 | D. | 加热H2SO3溶液 |
9.关于钠的叙述中,不正确的是( )
| A. | 钠是银白色金属,硬度很大 | B. | 金属钠的熔点很高 | ||
| C. | 金属钠通常保存在空气中 | D. | 钠的密度比水大 |
 ;(取代反应).
;(取代反应).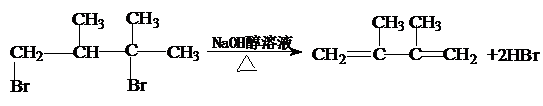 ; (消去反应).
; (消去反应). 将等物质的量的Cl2和CH4混合气体A.
将等物质的量的Cl2和CH4混合气体A.