题目内容
高纯硅生产流程如下: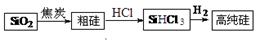
(1)由SiO2制粗硅的化学方程式是 ,该反应不能说明碳的非金属性强于硅,原因是 ,请写出一个能说明碳的非金属性强于硅的化学方程式 。
(2)900℃以上,H2与SiHCl3发生反应:SiHCl3(g)+ H2(g) Si(s) + 3HCl(g) ΔH>0。将一定量的反应物通入固定容积的密闭容器中进行反应。下列说法正确的是 (填字母)。
Si(s) + 3HCl(g) ΔH>0。将一定量的反应物通入固定容积的密闭容器中进行反应。下列说法正确的是 (填字母)。
a.在恒温条件下,若容器内压强不变,则该反应一定达到化学平衡状态
b.增大SiHCl3的用量,可提高SiHCl3的平衡转化率
c.升高温度可加快反应速率,且提高硅的产率
(3)该流程中可以循环使用的物质是 。
(1)SiO2+2C Si+2CO↑;非金属性是指非金属元素的单质在化学反应中得到电子的能力,而碳与二氧化硅反应所表现出来的是碳失去电子的能力(或还原性),因此不能说明碳的非金属性比硅强;Na2SiO3+2CO2+2H2O=2NaHCO3+H4SiO4↓或CO2+Na2SiO3+H2O=H2SiO3↓+Na2CO3。
Si+2CO↑;非金属性是指非金属元素的单质在化学反应中得到电子的能力,而碳与二氧化硅反应所表现出来的是碳失去电子的能力(或还原性),因此不能说明碳的非金属性比硅强;Na2SiO3+2CO2+2H2O=2NaHCO3+H4SiO4↓或CO2+Na2SiO3+H2O=H2SiO3↓+Na2CO3。
(2)a c (3)HCl、H2
解析试题分析:(1)SiO2+2C Si+2CO↑;非金属性是指非金属元素的单质在化学反应中得到电子的能力,而碳与二氧化硅反应所表现出来的是碳失去电子的能力(或还原性),因此不能说明碳的非金属性比硅强;Na2SiO3+2CO2+3H2O=2NaHCO3+H4SiO4↓或CO2+Na2SiO3+H2O=H2SiO3↓+Na2CO3
Si+2CO↑;非金属性是指非金属元素的单质在化学反应中得到电子的能力,而碳与二氧化硅反应所表现出来的是碳失去电子的能力(或还原性),因此不能说明碳的非金属性比硅强;Na2SiO3+2CO2+3H2O=2NaHCO3+H4SiO4↓或CO2+Na2SiO3+H2O=H2SiO3↓+Na2CO3
(2)从化学方程式来看,气体反应物和气体生成物的化学计量数不相等,即是一个气体体积在反应前后存在变化的化学反应,压强在反应过程中也存在变化,当不再变化时,说明达到平衡,a正确;增大SiHCl3的用量,可提高H2的平衡转化率,SiHCl3的平衡转化率反而减小。b错误;该反应正反应方向是吸热反应,升高温度向着吸热反应的方进行,平衡右移,c正确。(3)HCl、H2
考点:考查硅及其化合物的性质、化学方程式的属性、非金属性的强弱比较方法、化学平衡。


 ,可能含有CO
,可能含有CO
 的离子方程式为_____________________________________;
的离子方程式为_____________________________________;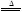 2KNO2+O2↑
2KNO2+O2↑ 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑ 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑