题目内容
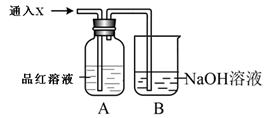
用如图所示装置可以收集以下几种气体(烧瓶位置不动)(填字母,下同);
①H2 ②SO2 ③CH4④ HCl ⑤ NH3 ⑥ NO ⑦H2S
(1)若烧瓶是干燥的,则由A口进气,可收集到的气体有 ,由B口进气,可收集的气体有 。
(2)若在烧瓶中充满水,可收集的气体有 ,气体由 口进入。
(3)若此装置用于净化气体,在烧瓶内装有洗涤液,则混合气体应由 口进入。
(1)①③⑤;②④⑦ (2)①③⑥ A (3)B
解析试题分析:(1)关键装置图可知,若烧瓶是干燥的,由A口进气收集气体,这说明该气体的密度小于空气的,因此符合条件的是氢气、甲烷和氨气,答案选①③⑤;由B口进气收集气体,这说明该气体的密度大于空气的,因此符合条件的是SO2、氯化氢和H2S,NO极易被氧化,不能用排空气法收集,答案选②④⑦。
(2)若在烧瓶中充满水,收集气体,说明气体不溶于水,和水与不反应,则符合条件氢气、甲烷和NO,则答案选①③⑥,此时气体由A口进入。
(3)当烧瓶中装入洗液,用于洗气时,要使洗气更充分,则气体应从B口进入烧瓶。
考点:考查气体的收集以及洗气瓶的使用等
点评:该题是高考中的常见题型,属于中等难度试题的考查。试题针对性强,注重答题的灵活性,有利于培养学生的实验能力和实验分析和评价能力。注意收集气体时常根据气体的密度、溶解性等性质,有时还要考虑与氧气的反应等问题,如NO与氧气反应,则只能用排水法收集。
考点:
点评:

下列气体中,既可用浓H2SO4干燥,又可用固体NaOH干燥的是
| A.Cl2 | B.NH3 | C.SO2 | D.O2 |
过氧化钙晶体[CaO2·8H2O]较稳定,呈白色,微溶于水,能溶于酸性溶液。广泛应用于环境杀菌、消毒等领域。
Ⅰ.过氧化钙晶体的制备。
工业上生产CaO2·8H2O的主要流程如下: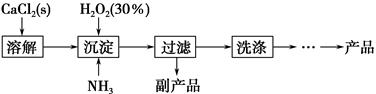
(1)用上述方法制取CaO2·8H2O的化学方程式是_________________________________。
(2)沉淀时常用冰水控制温度在10 ℃以下和通入过量的NH3,其可能原因分别是①__________________________;②_____________________________。
Ⅱ.过氧化钙晶体含量的测定。
准确称取0.300 0 g产品于锥形瓶中,加入30 mL蒸馏水和10 mL 2.000 mol·L-1 H2SO4,用0.020 0 mol·L-1 KMnO4标准溶液滴定至终点。重复上述操作两次。H2O2和KMnO4反应的离子方程式为2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O
滴定终点观察到的现象为_______________________________________。
(4)根据表中数据,计算产品中CaO2·8H2O的质量分数(写出计算过程)。
KMnO4标准溶液滴定数据
| 滴定次数 | 样品的质量/g | KMnO4溶液的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.300 0 | 1.02 | 24.04 |
| 2 | 0.300 0 | 2.00 | 25.03 |
| 3 | 0.300 0 | 0.20 | 23.24 |
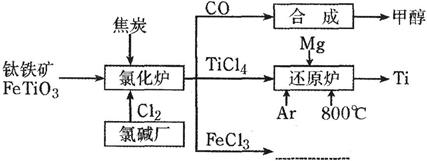



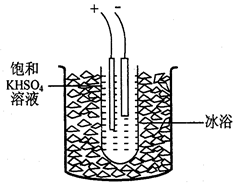
 I2+I-;2S2O32-+I2=2I- + S4O62-)
I2+I-;2S2O32-+I2=2I- + S4O62-)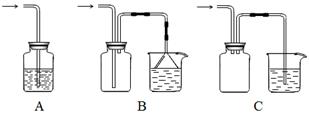

 N2O3(g),其平衡常数表达式为K = 。
N2O3(g),其平衡常数表达式为K = 。