题目内容
(10分)铜是一种重要的金属元素,铜元素与银元素同处第ⅠB族,+1价的铜和+1价的银都可形成二配位的络离子,如Ag(NH3)2+、AgCl2—等,含铜最丰富的天然资源是黄铜矿(CuFeS2)。
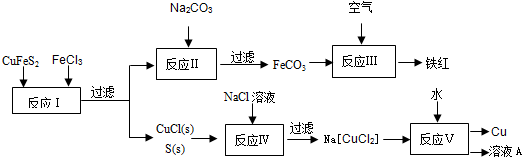
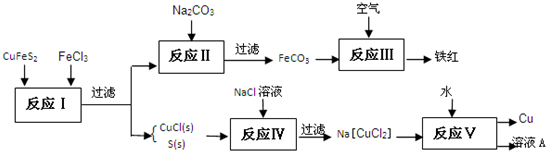
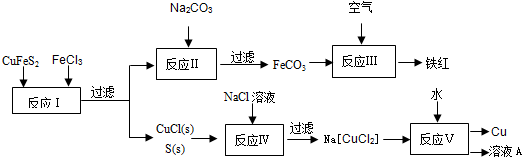
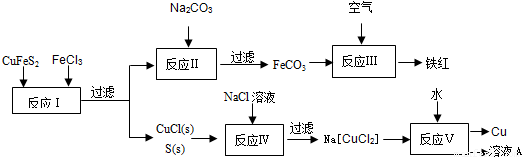
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜。这种方法的缺点是 、 。
|
|
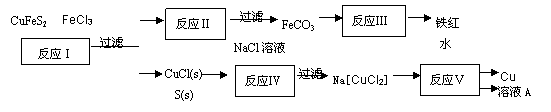 |
①写出反应Ⅰ中FeCl3与CuFeS2所发生反应的化学方程式: ;
②写出反应Ⅳ中发生反应的离子方程式: 。
③反应Ⅲ是FeCO3在空气中煅烧,写出化学方程式: 。
④反应Ⅴ所得溶液A中含有的溶质有 。
(10分除)
(1)SO2会导致大气污染 ,同时要消耗大量的热能 (各1分共2分)
|
(2)①CuFeS2 + 3FeCl3 = CuCl↓+ 4FeCl2 + 2S↓ ;2分
② Cl- + CuCl = [CuCl2]- 2分
③ 4FeCO3 + O2 == 4CO2 + 2Fe2O3 2分
④CuCl2、 NaCl 2分

练习册系列答案
相关题目