题目内容
4.短周期中的六种元素A、B、C、X、Y、Z,原子序数依次减小,其中X、Y、Z原子核外电子层数之和是5.X元素原子最外电子层上的电子数是Y和Z两种元素最外电子层上的电子数的总和;Y元素原子的最外层电子层上的电子数是它的电子层数的2倍,X和Z可以形成化合物XZ3;C与X处于同周期,B+与C2-的核外电子排布相同,A与B处于同周期,且形成BA型化合物.请回答:(1)Y元素的名称是碳;
(2)XZ3化合物的电子式是
 ;
;(3)A、B、C的离子半径由大到小的顺序为Cl->O2->Na+(用元素离子符号表示);
(4)用XZ4A制备XZ3的化学反应方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2.
(5)元素组成的化合物XZ5YC3和足量的化合物BCZ反应的离子方程式为NH4++HCO3-+2OH-═NH3•H2O+CO32-+H2O.
分析 六种短周期元素A、B、C、X、Y、Z原子序数依次减小,Y元素原子的最外电子层电子数是它的电子层数的2倍,结合原子序数可知,Y只能处于第二周期,故Y原子最外层电子数为4,则Y为C元素;X、Y、Z原于核外电子层数之和是5,故X、Z电子层之和为3,Z的原子序数最小,Z处于第一周期、X处于第二周期,故Z为H元素;X元素原子最外电子层上的电子数是Y和Z两种元素最外电子层上的电子数的总和,故X原子最外层电子数之和为4+1=5,则X为N元素;C与X处于同周期,B+与C2-的核外电子排布相同,则C为O元素,B原子序数大于氧元素,则B为Na元素;A与B处于同周期,且可形成BA型化合物,A为-1价,则A为Cl元素,据此解答.
解答 解:六种短周期元素A、B、C、X、Y、Z原子序数依次减小,Y元素原子的最外电子层电子数是它的电子层数的2倍,结合原子序数可知,Y只能处于第二周期,故Y原子最外层电子数为4,则Y为C元素;X、Y、Z原于核外电子层数之和是5,故X、Z电子层之和为3,Z的原子序数最小,Z处于第一周期、X处于第二周期,故Z为H元素;X元素原子最外电子层上的电子数是Y和Z两种元素最外电子层上的电子数的总和,故X原子最外层电子数之和为4+1=5,则X为N元素;C与X处于同周期,B+与C2-的核外电子排布相同,则C为O元素,B原子序数大于氧元素,则B为Na元素;A与B处于同周期,且可形成BA型化合物,A为-1价,则A为Cl元素,
(1)由上述分析可知,Y为碳元素,故答案为:碳;
(2)NH3化合物的电子式是 ,故答案为:
,故答案为: ;
;
(3)电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径Cl->O2->Na+,故答案为:Cl->O2->Na+;
(4)化合物XZ4A为NH4Cl,制备氨气的方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2,故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2;
(5)化合物NH5CO3为NH4HCO3,与足量NaOH反应生成NH3•H2O、碳酸钠、H2O,反应的离子方程式为:NH4++HCO3-+2OH-═NH3•H2O+CO32-+H2O,
故答案为:NH4++HCO3-+2OH-═NH3•H2O+CO32-+H2O.
点评 本题考查结构性质位置关系运用、半径比较、电子式、离子方程式等,难度不大,推断元素是解题关键,注意基础知识的理解掌握.

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案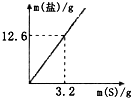 资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3.某化学兴趣小组进行该实验时,却检测到生成的盐中含有SO42-.
资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3.某化学兴趣小组进行该实验时,却检测到生成的盐中含有SO42-.(1)兴趣小组同学认为,上述反应的生成物可能与反应温度(T),KOH溶液的浓度(C)有关.他们做了如下对比实验(每次反应中硫粉的质量、KOH溶液的体积均相同).
| 实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| T/℃ | 50 | 60 | 70 | 80 | 90 | |||
| c/mol•L-1 | 1.0 | 3.0 | 4.0 | 5.0 | 6.0 |
(2)兴趣小组设计实验对上述反应中生成的盐的成分进行探究.他们提出如下假设,请你根据氧化还原反应的规律,完成假设二和假设三:
假设一:生成的盐是K2S和K2SO3;
假设二:生成的盐是K2S和K2SO4;
假设三:生成的盐是K2S,K2SO3和K2SO4;
(3)请你设计实验验证上述假设一.完成下表中内容.(除了硫粉与热的KOH溶液的反应液之外,可供选择的药品有稀硝酸,稀盐酸等;已知:6H++SO32-+2S2-=3S+3H2O)
| 实验方案(不要求写出具体操作过程) | 预期实验现象和结论 |
| 在反应液中加入足量的稀盐酸 | 若溶液变浑浊且没有气体溢出(或:若没有气体溢出),则假设一成立;若溶液中有气体逸出,则假设一不成立 |
(5)请分析上述反应中有K2SO4生成的可能原因是:亚硫酸钾具有还原性,很容易被氧气氧化为硫酸钾.
| 元素代号 | A | B | C | D | E | F | G | H | I | J | K |
| 常见化合价 | -1 | -2 | +5、-3 | +4、-4 | +6、+4、-2 | +4、-4 | +5、-3 | +3 | +2 | +1 | +1 |
| 原子半径/pm | 71 | 74 | 75 | 77 | 102 | 117 | 110 | 143 | 160 | 186 | 152 |
(1)E元素在周期表中位置是第二周期IA族.
(2)A、H、J对应离子的半径由大到小的顺序是F->Na+>Al3+(填离子符号)
(3)A与J所形成的化合物中含有离子键(填“离子”或“共价”)
(4)写出DB2的电子式:
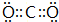 .
.(5)写出D的最高价氧化物与J的最高价氧化物对应水化物X的溶液(足量)发生反应的离子方程式:CO2+OH-=HCO3-.
| A. | NH4Br的电子式: | B. | S2-的结构示意图: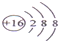 | ||
| C. | 氮气的结构式:N═N | D. | 乙烷的分子式:CH3CH3 |
| A. | Cu $\stackrel{浓硝酸}{→}$ Cu(NO3)2 | B. | Cu$\stackrel{AgNO_{3}}{→}$ Cu(NO3)2 | ||
| C. | Cu $\stackrel{Cl_{2}}{→}$ CuCl2$\stackrel{稀硝酸}{→}$Cu(NO3)2 | D. | Cu$\stackrel{空气}{→}$ CuO $\stackrel{HNO_{3}}{→}$ Cu(NO3)2 |
| A. | X与W形成化合物稳定性一定强于Z与W形成化合物 | |
| B. | Y、Z两元素的简单离子半径Y>Z | |
| C. | X、Y、Z对应气态氢化物的热稳定性和还原性强弱顺序一致 | |
| D. | Y元素最高价氧化物对应水化物的化学式为HYO4 |
| A. | 碳素钢 | B. | 水银 | C. | 青铜 | D. | 黄铜 |
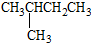
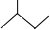
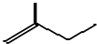 C5H10
C5H10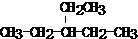
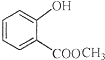 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.