题目内容
已知某酸性溶液中含有Ba2+、Fe3+,则下列能与上述离子共存的离子组是( )
A. CO32﹣、SO42﹣、NH4+、Na+ B. Cl﹣、SCN﹣、NO3﹣、Cu2+
C. Br﹣、I﹣、Mg2+、Na+ D. H+、Cl﹣、NO3﹣、Al3+
练习册系列答案
相关题目
为提纯下列物质(括号内为少量杂质),所选用的除杂式试剂和分离方法正确的是( )
提纯物质 | 除杂试剂 | 分离法 | |
A | KCl溶液(FeCl3) | 氨水 | 过滤 |
B | 乙酸乙酯(乙酸) | 乙醇和浓硫酸 | 分液 |
C | Fe粉(Al粉) | NaOH溶液 | 过滤 |
D | 乙醇(H2O) | 金属钠 | 蒸馏 |
A. A B. B C. C D. D
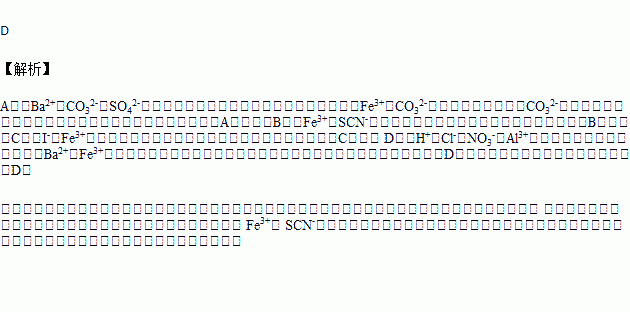



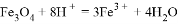


 2OH -+ H2↑
2OH -+ H2↑ Cr2O72- + H2O向右移动
Cr2O72- + H2O向右移动 2K2Cr2O7 + 4KOH + 2H2↑+ O2↑
2K2Cr2O7 + 4KOH + 2H2↑+ O2↑