题目内容
17.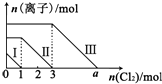 向仅含Fe2+、I-、Br -的溶液通入适量氯气,溶液中这三种离子的物质的量的变化如图所示.下列说法中正确的是( )
向仅含Fe2+、I-、Br -的溶液通入适量氯气,溶液中这三种离子的物质的量的变化如图所示.下列说法中正确的是( )| A. | 线段Ⅲ代表Fe2+的变化情况 | B. | 线段Ⅰ代表Br -的变化情况 | ||
| C. | 原混合溶液中n(FeBr2)=4mol | D. | a数值等于6 |
分析 向仅含Fe2+、I-、Br-的溶液中通入适量氯气,根据还原性:I->Fe2+>Br-,首先发生反应:2I-+Cl2═I2+2Cl-,I-反应完毕,再发生反应:2Fe2++Cl2═2Fe3++2Cl-,Fe2+反应完毕,最后发生反应:2Br-+Cl2═Br2+2Cl-,故线段Ⅰ代表I-的变化情况,线段Ⅱ代表Fe2+的变化情况,线段Ⅲ代表Br-的变化情况;
由通入氯气可知,根据反应离子方程式可知溶液中n(I-)=2n(Cl2)=2mol,溶液中n(Fe2+)=2n(Cl2)=2×(3mol-1mol)=4mol,Fe2+反应完毕,
根据电荷守恒可知n(I-)+n(Br-)=2n(Fe2+),故n(Br-)=2n(Fe2+)-n(I-)=2×4mol-2mol=6mol,根据溴离子判断溶液中n(FeBr2);根据离子方程式计算溴离子反应需要的氯气的物质的量,据此计算a的值.
解答 解:向仅含Fe2+、I-、Br-的溶液中通入适量氯气,根据还原性:I->Fe2+>Br-,首先发生反应:2I-+Cl2=I2+2Cl-,I-反应完毕,再发生反应:2Fe2++Cl2=2Fe3++2Cl-,Fe2+反应完毕,最后发生反应:2Br-+Cl2=Br2+2Cl-,故线段Ⅰ代表I-的变化情况,线段Ⅱ代表Fe2+的变化情况,线段Ⅲ代表Br-的变化情况;
由通入氯气可知,根据反应离子方程式可知溶液中n(I-)=2n(Cl2)=2mol,溶液中n(Fe2+)=2n(Cl2)=2×(3mol-1mol)=4mol,Fe2+反应完毕,
根据电荷守恒可知n(I-)+n(Br-)=2n(Fe2+),
故n(Br-)=2n(Fe2+)-n(I-)=2×4mol-2mol=6mol,
A、由上述分析可知,线段Ⅲ代表Br-的变化情况,故A错误;
B、由上述分析可知,线段I代表I-的变化情况,故B错误;
C、溶液中n(Br-)=6mol,所以原混合溶液中n(FeBr2)=3mol,故C错误;
D、上述分析可知,溶液中n(Br-)=2n(Fe2+)-n(I-)=2×4mol-2mol=6mol,根据2Br-+Cl2═Br2+2Cl-可知,溴离子反应需要的氯气的物质的量为3mol,故a=3+3=6,故D正确;
故选:D.
点评 本题考查氧化还原反应计算、氧化还原反应先后顺序、氧化性和还原性强弱比较,综合性较强,难度较大,清楚反应过程是解题关键.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 向NH4Al(S04)2溶液中滴加过量Ba(OH)2溶液:2Ba2++40H-+2S042-+Al3+=2BaS04↓+2H20+Al02- | |
| B. | 向NaHS04溶液中滴Ba(OH)2溶液至S042-完全沉淀:2 H++S042-+Ba2++20H-=BaS04↓+2H20 | |
| C. | 向0.1mol.L-l、pH=l的NaHA溶液中加入NaOH溶液:HA-十OH-=A2-+H20 | |
| D. | 向1L lmol.L-1的FeBr2溶液中通等物质的量Cl2:2Cl2+2Fe2++2Br-=4Cl-十2Fe3++Br2 |
①熟石灰可用来改良土壤酸性 ②氦气可做保护气
③KMnO4可作消毒剂 ④蒸馒头时可用NaOH来除去面团中发酵产生的酸
⑤可用Al(OH)3治疗胃酸过多 ⑥工业上可用Na2CO3来制肥皂
⑦工业上可用铁桶盛放波尔多液 ⑧家庭中可用NaNO2作调味品.
| A. | ②④⑤⑦ | B. | ②③⑤ | C. | ①②③⑤ | D. | ①⑤⑥⑧ |
| A. | 等质量的Na2CO3、NaHCO3与足量的盐酸反应,在相同条件下NaHCO3产生CO2的体积大 | |
| B. | 等物质的量的Na2CO3和NaHCO3与同浓度的足量盐酸反应,Na2CO3所消耗盐酸的体积是NaHCO3的两倍 | |
| C. | 将石灰水加入NaHCO3溶液中不会产生沉淀,加入Na2CO3溶液中会产生沉淀 | |
| D. | 等物质的量的NaHCO3和Na2CO3与足量Ba(OH)2溶液反应,所得沉淀的质量相等 |
| 编号 | 金属(粉末状)mol | 酸的浓度及体积 | 反应温度(℃) |
| A | Mg,0.1 | 6mol/L硝酸10ml | 80 |
| B | Mg,0.1 | 3mol/L盐酸10ml | 60 |
| C | Fe,0.1 | 3mol/L盐酸10ml | 60 |
| D | Mg,0.1 | 3mol/L硫酸10ml | 60 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 电解饱和食盐水可制得金属钠 | B. | 海水提溴涉及到氧化还原反应 | ||
| C. | 海带提碘只涉及物理变化 | D. | 海水提镁不涉及复分解反应 |
| A. | 78g由Na2S和Na2O2组成的固体混合物,含有的阴离子数为NA | |
| B. | 标准状况下,22.4L CCl4中含有的分子数为NA | |
| C. | 将1mol FeCl3水解制成胶体,所得胶体中含有的胶体粒子数为NA | |
| D. | 1mol/L NaOH溶液中含有的Na+数目为NA |
| A. | H+、Ca2+、CO32-、Cl- | B. | H+、Fe2+、NO3-、OH- | ||
| C. | K+、Na+、Cl-、OH- | D. | Cu2+、Ba2+、Cl-、SO42- |