题目内容
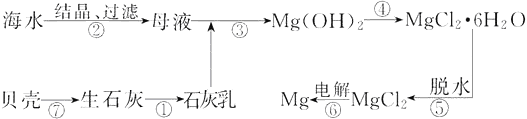
【题目】从海水中提取镁的工业流程如图所示,下列说法不正确的是
A. 用此法提取镁的优点之一是原料来源丰富
B. 在实验室进行②的操作需用到坩埚、坩埚钳、玻璃棒、酒精灯
C. 步骤⑥电解MgCl2时,副产物Cl2可以循环利用
D. 上述工艺流程中的反应未涉及置换反应
【答案】B
【解析】
提取镁的工艺流程中发生的反应有:CaCO3 ![]() CaO+CO2↑,CaO+H2O=Ca(OH)2,Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2,Mg(OH)2+2HCl=MgCl2+2H2O,MgCl2
CaO+CO2↑,CaO+H2O=Ca(OH)2,Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2,Mg(OH)2+2HCl=MgCl2+2H2O,MgCl2![]() Mg+Cl2↑,以此解答该题。
Mg+Cl2↑,以此解答该题。
A、海水在地球上含量丰富,海水中含有大量的镁,提取镁的原料来源丰富,故A正确;B.实验操作②是过滤,过滤时需要的仪器有烧杯、玻璃棒、漏斗、铁架台,故B错误; C、工业上用电解熔融氯化镁的方法冶炼Mg,副产物Cl2可以制得盐酸,参与循环利用,故C正确;D、根据上述分析,上述工艺流程中的反应未涉及置换反应,故D正确;故选B。

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目