题目内容
【题目】二氧化硫是危害最为严重的大气污染物之一,它主要来自化石燃料的燃烧,研究CO催化还原SO2的适宜条件,在燃煤电厂的烟气脱硫中具有重要价值。
Ⅰ.从热力学角度研究反应
(1)C(s)+O2(g)= CO2(g) ΔH1=-393.5 kJ·mol-1
CO2(g)+C(s)=2CO(g) ΔH2=+172.5kJ·mol-1
S(s) +O2(g)= SO2(g) ΔH3=-296.0kJ·mol-1
请写出CO 还原SO2的热化学方程式___________________________________。
(2)对于CO还原SO2的可逆反应,下列说法正确的是_____________。
A.在恒温恒容条件下,若反应体系压强不变,则反应已达到平衡状态
B.平衡状态时,2v正(CO)=v逆(SO2)
C.其他条件不变,增加SO2的浓度,CO的平衡转化率增大
D.在恒温恒压的容器中,向达到平衡状态的体系中充入N2,SO2的平衡转化率不变
Ⅱ.探究合适的反应条件
向反应器中通入含3%SO2、6%CO和91%N2的烟气,用碘量法测定反应前后烟气中SO2的含量,反应温度区间均为300℃~500℃。
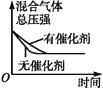
(1)催化剂和温度对反应的影响
烟气流量为0.03 L/min,分别在3种不同催化剂条件下进行实验,实验结果如下图所示。

根据上图示结果,烟气除硫时选用最合适催化剂是_____________,反应温度是_______________。
(2)烟气流速对反应的影响
选用同样的催化剂,分别在三种烟气流量情况下进行实验,实验结果的数据见下表。
温度(℃) | 300 | 400 | 500 | |
SO2转化率 | 流量0.03 L/min | 25.00% | 71.40% | 65.00% |
流量 0.06 L/min | 20% | 74.20% | 62.60% | |
流量0.09 L/min | 18% | 76.30% | 60% | |
分析上表数据,①在300℃时,SO2的转化率随烟气流量变化的关系是______________,其原因可能是____________;②在400℃时,SO2的转化率随烟气流量增大而增大的原因是___________________。
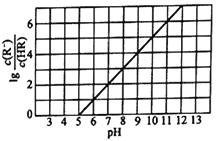
Ⅲ.工业上还用Na2SO3溶液吸收SO2,将烟气通入1.0 mol·L-1的Na2SO3溶液,当溶液pH约为6 时,吸收SO2的能力显著下降,此时溶液中c(HSO3-)∶(SO32-)=____________。(已知H2SO3的K1
【答案】 2CO(g)+SO2(g)==2CO2(g)+S(s) ΔH=-270.0kJ·mol-1 AC 3#催化剂 400℃ 烟气流量越大,SO2的转化率越小 300℃时,催化剂活性不好,反应速率慢,烟气流速越小,气体和催化剂接触时间越长,SO2转化率越高 400℃时,催化剂活性好,反应速率快,烟气流速越大,反应物浓度越大,反应正向进行越彻底,SO2 转化率越高 10
【解析】I. (1). 已知 ① C(s)+O2(g)= CO2(g) ΔH1=-393.5 kJ·mol-1、② CO2(g)+C(s)=2CO(g) ΔH2=+172.5kJ·mol-1、③ S(s) +O2(g)= SO2(g) ΔH3=-296.0kJ·mol-1,根据盖斯定律,①-②-③得:2CO(g)+SO2(g)=2CO2(g)+S(s) ΔH=-270.0kJ·mol-1,故答案为:2CO(g)+SO2(g)=2CO2(g)+S(s) ΔH=-270.0kJ·mol-1;
(2). A. 2CO(g)+SO2(g)=2CO2(g)+S(s)是反应前后气体体积不相等的可逆反应,在恒温恒容条件下,若反应体系压强不变,说明反应达到平衡状态,故A正确;B. 达到平衡状态时,v正(CO)=2v逆(SO2),故B错误;C. 增大SO2的浓度,平衡正向移动,CO的转化率增大,故C正确;D. 在恒温恒压的容器中,向达到平衡状态的体系中充入N2,容器的体积增大,相当于减小压强,平衡逆向移动,SO2的平衡转化率减小,故D错误;答案选:AC;
II. (1). 据图可知,使用3#催化剂、在400℃时,SO2的转化率最大,故答案为:3#催化剂;400℃;
(2). ①.由表中数据可知,在300℃时,烟气的流量越大,SO2的转化率越小,结合图象可知,在300℃时,催化剂的催化活性较低,所以在此温度下反应速率慢,烟气的流速越小,气体和催化剂接触的时间越长,SO2的转化率越高,故答案为:烟气流量越大,SO2的转化率越小;300℃时,催化剂活性不好,反应速率慢,烟气流速越小,气体和催化剂接触时间越长,SO2转化率越高;
②. 据图可知,在400℃时,催化剂活性最好,此温度下反应速率最快,烟气流速越大,反应物浓度越大,反应正向进行越彻底,SO2的转化率越高,故答案为:400℃时,催化剂活性好,反应速率快,烟气流速越大,反应物浓度越大,反应正向进行越彻底,SO2 转化率越高;
III. 溶液pH=6,c(H+)=10-6mol/L,H2SO3的二级电离常数K2=![]() =1.0×10-7,
=1.0×10-7,![]() =
=![]() =
=![]() =10,故答案为:10。
=10,故答案为:10。

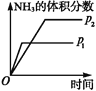
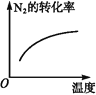
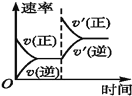
【题目】对于可逆反应N2(g)+3H2(g) ![]() 2NH3(g)ΔH<0,下列研究目的和示意图相符的是( )
2NH3(g)ΔH<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
研究目的 | 压强对反应的影响(p2>p1) | 温度对反应的影响 | 平衡体系中增加N2浓度对反应的影响 | 催化剂对反应的影响 |
示意图 |
|
|
|
|
A. A B. B C. C D. D