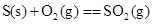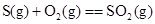题目内容
已知:① S(单斜,s)+O2(g) = SO2(g) △H1=-297.16 kJ·mol-1
② S(正交,s)+O2(g) = SO2(g) △H2=-296.83 kJ·mol-1
③ S(单斜,s) = S(正交,s) △H3
下列说法正确的是( )
② S(正交,s)+O2(g) = SO2(g) △H2=-296.83 kJ·mol-1
③ S(单斜,s) = S(正交,s) △H3
下列说法正确的是( )
| A.S(单斜)和S(正交)互为同分异构体 |
| B.△H3= + 0.33 kJ·mol-1 ,单斜硫转化为正交硫的反应是吸热反应 |
| C.S(单斜,s) = S(正交,s) △H3<0,正交硫比单斜硫稳定 |
| D.S(单斜,s) = S(正交,s) △H3>0,单斜硫比正交硫稳定 |
C
试题分析:S(单斜)和S(正交)互为同素异形体,A不正确;根据盖斯定律可知①-②即得到S(单斜,s) =S(正交,s),所以该反应的反应热△H3=-297.16 kJ/mol+296.83 kJ/mol=-0.33kJ/mol,即该反应是放热反应,所以单斜硫比正交硫的能量高。能量越低越稳定,则正交硫比单斜硫稳定,C正确,BD错误,答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题,试题基础性强,侧重对学生基础知识的巩固与训练,主要是考查学生灵活运用基础知识解决实际问题的能力,也有助于培养学生的逻辑推理能力和抽象思维能力。

练习册系列答案
相关题目

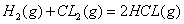 )在光照和点燃条件的△H相同
)在光照和点燃条件的△H相同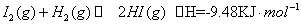
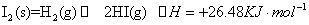
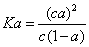 。若加入少量醋酸钠固体,则CH3COOH;—一CH3COO -十H+向左移动,a减小,Ka变小若加入少量醋酸钠固体,则
。若加入少量醋酸钠固体,则CH3COOH;—一CH3COO -十H+向左移动,a减小,Ka变小若加入少量醋酸钠固体,则
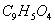 十H+向左移动,a减小,Ka变小
十H+向左移动,a减小,Ka变小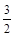 O2(g)==CO2(g)+2H2O(l);△H=-725.8kJ· mol—1
O2(g)==CO2(g)+2H2O(l);△H=-725.8kJ· mol—1