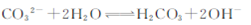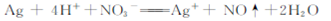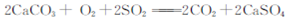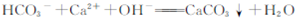题目内容
向盛有NaHSO4溶液的烧杯中不断滴Ba(OH)2溶液,随着Ba(OH)2溶液的不断滴入,溶液中产生的沉淀量与pH变化情况正确的是 
A
解析试题分析:硫酸氢钠与氢氧化钡反应:当溶液显示中性时,反应的化学方程式为:2NaHSO4+Ba(OH)2=Na2SO4+BaSO4↓+2H2O,溶液中硫酸根离子没有完全沉淀,即沉淀没有达到最大量;当沉淀达到最大量时,反应的化学方程式为:NaHSO4+Ba(OH)2=NaOH+BaSO4↓+H2O,此时溶液中氢氧根离子过量,溶液显示碱性,溶液的pH>7,满足以上关系的图象为A.故选:A.
考点:考查由图表计算相关物理量的相关知识点

练习册系列答案
相关题目
下列各组物质中,因为反应条件或用量不同而发生不同化学反应的是( )
①C与O2 ②Na与O2 ③Fe与Cl2 ④AlCl3溶液与氨水
⑤CO2与NaOH溶液 ⑥Cu与硝酸 ⑦AgNO3溶液与氨水
| A.除③外 | B.除③⑦外 | C.除③④外 | D.除⑥⑦外 |
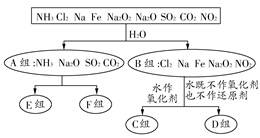
某溶液中可能含有K+、NH4+、Ba2+、SO42一、I一、 CO32一。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和CCl4振荡后静置,下层呈无色。为确定该溶液的组成,还需检验的离子是 ( )
| A.K+ | B.SO42一 | C.Ba2+ | D.NH4+ |
在25℃的条件下,下列各组离子一定能在指定环境中大量共存的是
A.在c(H+)=10-10 mol/L的溶液中: Al3+、NH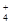 、Cl- 、NO 、Cl- 、NO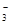 |
B.pH=13的溶液中:K+ 、Na+、SO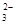 、Cl- 、Cl- |
C.pH=2的溶液中: K+、NH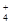 、Cl-、ClO- 、Cl-、ClO- |
D.甲基橙呈红色的溶液中:Fe3+、Na+ 、SO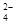 、CO 、CO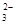 |
下列指定反应的离子方程式正确的是
| A.Cu溶于稀硝酸:Cu+2H++NO3-=Cu2++NO2↑+H2O |
| B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ |
| C.用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D.向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3- |
在下列溶液中,一定能大量共存的离子组是
A.常温下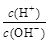 =1012的溶液中:Fe2+、Mg2+、NO3-、Cl- =1012的溶液中:Fe2+、Mg2+、NO3-、Cl- |
| B.含有大量Al3+的溶液中:SO42-、S2-、AlO2-、ClO-、 |
| C.能使pH试纸显蓝色的溶液中:K+、Ba2+、Cl-、Br- |
| D.常温下,在由水电离出的c(H+)=1×10-13 mol·L-1的溶液中:K+、Fe3+ 、Cl-、SO42- |