题目内容
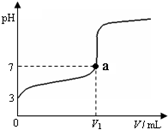
常温下,向20 mL x mol·L-1 CH3COOH溶液中逐滴加入等物质的量浓度的NaOH溶液,混合液的pH随NaOH溶液的体积(V)的变化关系如图所示(忽略温度变化)。下列说法中正确的是

| A.上述 CH3COOH溶液中:c(H+)=1×10-3 mol·L-1 |
| B.图中V1 >20 mL |
| C.a点对应的溶液中:c (CH3COO-)=c (Na+) |
| D.当加入NaOH溶液的体积为20 mL时,溶液中:c (CH3COOH) + c (H+)>c (OH-) |
AC
A:CH3COOH溶液的pH=3,也就是c(H+)=1×10-3 mol·L-1,正确
B:当酸碱等浓度等体积恰好中和时,生成CH3COONa溶液,水解呈碱性,故当pH=7时,需要V1 <20 mL,不正确
C:由电荷守恒可知c(H+)+c(Na+)=c (CH3COO-)+c (OH-),a点呈中性,c(H+)=c (OH-),故c(Na+)=c (CH3COO-),正确
D:此时溶液为CH3COONa溶液,存在电荷守恒:c(H+)+c(Na+)=c (CH3COO-)+c (OH-)及物料守恒:c(Na+)=c (CH3COO-)+c (CH3COOH),将后式代入前式可知c (CH3COOH) + c (H+)=c (OH-),不正确
答案为AC
B:当酸碱等浓度等体积恰好中和时,生成CH3COONa溶液,水解呈碱性,故当pH=7时,需要V1 <20 mL,不正确
C:由电荷守恒可知c(H+)+c(Na+)=c (CH3COO-)+c (OH-),a点呈中性,c(H+)=c (OH-),故c(Na+)=c (CH3COO-),正确
D:此时溶液为CH3COONa溶液,存在电荷守恒:c(H+)+c(Na+)=c (CH3COO-)+c (OH-)及物料守恒:c(Na+)=c (CH3COO-)+c (CH3COOH),将后式代入前式可知c (CH3COOH) + c (H+)=c (OH-),不正确
答案为AC

练习册系列答案
相关题目