题目内容
【题目】已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2![]() 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
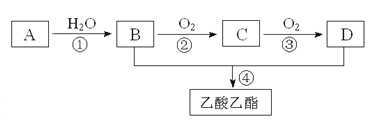
回答下列问题:
(1)写出A的电子式___________。
(2)B、D分子中的官能团名称分别___________、___________。
(3)写出下列反应的反应类型:①___________,②___________,④___________。
(4)写出下列反应的化学方程式:
①_____________________________________。
②_____________________________________。
④_____________________________________。
【答案】![]() 羟基 羧基 加成反应 氧化反应 取代反应 CH2=CH2+H2O
羟基 羧基 加成反应 氧化反应 取代反应 CH2=CH2+H2O![]() CH3CH2OH 2CH3CH2OH + O2
CH3CH2OH 2CH3CH2OH + O2 ![]() 2CH3CHO + 2H2O CH3COOH + CH3CH2OH
2CH3CHO + 2H2O CH3COOH + CH3CH2OH![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
【解析】
A的产量通常衡量一个国家的石油化工水平,则A应为CH2=CH2;A与水在一定条件下发生加成反应生成CH3CH2OH,乙醇在Cu或Ag作催化剂条件下发生氧化反应生成CH3CHO,CH3CHO可进一步氧化为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成乙酸乙酯。综上所述,A为CH2=CH2,B为CH3CH2OH,C为CH3CHO,D为CH3COOH。
(1)A为CH2=CH2,电子式为:![]() ,故填:
,故填:![]() ;
;
(2)B为CH3CH2OH,D为CH3COOH,分别含有的官能团为羟基和羧基,故填:羟基;羧基;
(3)反应①为CH2=CH2与水在一定条件下发生加成反应生成CH3CH2OH,反应②是CH3CH2OH在Cu或Ag作催化剂、加热条件下发生氧化反应生成CH3CHO,反应④是乙醇与乙酸在浓硫酸、加热条件下发生酯化反应生成乙酸乙酯,故填:加成反应、氧化反应、酯化反应;
(4)①反应方程式为CH2=CH2+ H2O![]() CH3CH2OH;
CH3CH2OH;
②反应方程式为2CH3CH2—OH + O2![]() 2CH3CHO + H2O;
2CH3CHO + H2O;
④反应方程式为CH3CH2OH+CH3COOH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O

【题目】有四种短周期元素,它们的结构、性质等信息如下表所述:
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | B与A同周期,其最高价氧化物的水化物呈两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
请根据表中信息填写:
(1)A原子的核外电子排布式______。
(2)离子半径:B____A(填“大于”或“小于”)。
(3)C原子的电子排布图是____,其原子核外有___个未成对电子,能量最高的电子为___轨道上的电子,其轨道呈____形。
(4)D原子电子所占原子轨道数为_______个,D﹣的结构示意图是_____。
(5)BD3的水溶液显______性,原因_____________________(用离子方程式表示)。