��Ŀ����
����Ŀ��һ����˵����һ��δ֪�л���ṹ�IJⶨ��Ҫ�������¼������棺
��ȷ����Է���������
�ڲⶨԪ����ɣ�����ͱ�������
���о����л���ĸ������ʣ�
��ȷ���ṹ��
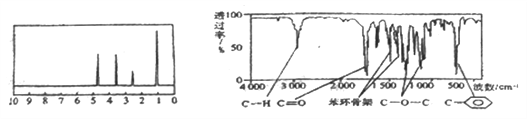
��1����Է���������ȷ��һ�����������������ܶȷ��ȡ�ij�л���![]() ������ͼ��ʾ����Է������������72�����Ԫ�صIJⶨ������Ԫ�ط����ǣ�Ҳ�ɲ���ȼ�շ�����ȡ
������ͼ��ʾ����Է������������72�����Ԫ�صIJⶨ������Ԫ�ط����ǣ�Ҳ�ɲ���ȼ�շ�����ȡ![]()
![]() �������������г��ȼ�գ�������ͨ��Ũ�����Ũ�������������
�������������г��ȼ�գ�������ͨ��Ũ�����Ũ�������������![]() ��ʣ������ͨ����ʯ�ң���ʯ�ҵ���������
��ʣ������ͨ����ʯ�ң���ʯ�ҵ���������![]() ����
����![]() �ķ���ʽΪ______��
�ķ���ʽΪ______��
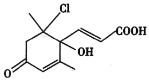
��2���˴Ź����׳�������̼�ף�����Ҫ�ⶨ�����о��в�ͬ�ص��![]() ��
��![]() ���������������������
���������������������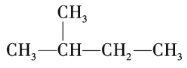 ����
����![]() �����ĸ��壬��߱�Ϊ
�����ĸ��壬��߱�Ϊ![]() ��
��![]() �����ĸ��壬��߱�Ϊ
�����ĸ��壬��߱�Ϊ![]() ���л���
�����![]() ��
��![]() ���������壬��߱�Ϊ
���������壬��߱�Ϊ![]() ��������һ���塣��д���л���
��������һ���塣��д���л���![]() �Ľṹ��ʽ��______��
�Ľṹ��ʽ��______��
��3��![]() ��һ�ȴ�����______�֣����ȴ�����______�֡�
��һ�ȴ�����______�֣����ȴ�����______�֡�
���𰸡�![]()
 1 2
1 2
��������
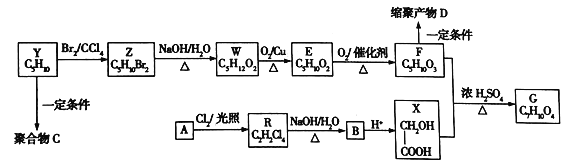
��1��3.6gA���������������ȼ�պ�ͨ��Ũ���ᣬŨ��������5.4g��Ũ�������յ��Ƿ�Ӧ������ˮ��ʣ������ͨ����ʯ�ң���ʯ������11g����ʯ�����յ��Ƕ�����̼������Ԫ���غ��֪A��C��H����������������ȷ��A����Ԫ�ص���������ȷ������ʽ��
��2������������Ϣ��֪��A̼���������壬��߱�Ϊ4��1��˵�������������ֲ�ͬ������̼���Ҹ�����Ϊ4��1��������һ���壬˵��ֻ��һ�ֻ�������ԭ�ӣ��ݴ�д�ṹ��
��3�����ݵ�Ч�ⷨ���з�����
��1��ȼ�պ����ͨ��Ũ���ᣬ����5.4g����ȼ�����ɵ�ˮΪ5.4g�����ʵ���Ϊ0.3mol��˵��A����H�����ʵ���Ϊ0.6mol��ͨ����ʯ�ң�����11g����ʯ�����յ�ΪCO2����ȼ�����ɵ�CO2���ʵ���Ϊ0.25mol��˵��A����C�����ʵ���Ϊ0.25mol������ͼ��ʾ����Է������������72����A����Է�������Ϊ72��![]()
![]() �����ʵ���Ϊ0.05mol������1��A�����е�̼ԭ����Ϊ
�����ʵ���Ϊ0.05mol������1��A�����е�̼ԭ����Ϊ![]() =5����ԭ����Ϊ
=5����ԭ����Ϊ![]() =12��A����Է�������Ϊ72������A�ķ���ʽΪ
=12��A����Է�������Ϊ72������A�ķ���ʽΪ![]() ��
��
��2�����![]() ��
��![]() ���������壬��߱�Ϊ
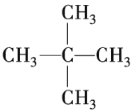
���������壬��߱�Ϊ![]() ��˵��A��������̼ԭ�ӣ�������һ���壬˵��ֻ��һ����ԭ�ӣ�����A�Ľṹ��ʽΪ
��˵��A��������̼ԭ�ӣ�������һ���壬˵��ֻ��һ����ԭ�ӣ�����A�Ľṹ��ʽΪ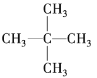 ��
��
��3��A�����е���ԭ�Ӷ��ǵ�Ч�⣬����ֻ��һ��һ�ȴ����������е�2����ԭ�ӱ���ԭ�Ӵ��棬������ͬһ��̼ԭ���ϵ�2����ԭ�ӱ���ԭ��ȡ����Ҳ�����Dz�̼ͬԭ���ϵ���ԭ�ӱ���ԭ��ȡ�������Զ��ȴ�����2�֡�

 ����Ӣ��ϵ�д�
����Ӣ��ϵ�д�����Ŀ���±��Ǽ������᳣���µĵ���ƽ�ⳣ����
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8��10-5 | K1=4.3��10-7 K2=5.6��10-11 | K1=9.1��10-8 K2=1.1��10-12 | K1=7.5��10-3 K2=6.2��10-8 K3=2.2��10-13 |
������˵���в���ȷ���ǣ�������
A. ̼�������ǿ��������
B. ��Ԫ�����������Ҫ�ɵ�һ���������
C. �����£���ˮϡ�ʹ��ᣬ![]() ����
����
D. ��������Һ�м�����NaOH��Һ�����볣������