题目内容
下列溶液中,一定能大量共存的粒子组是( )
| A.pH=1的溶液中:K+、Cr2O72—、CH3CH2OH、SO32— |
| B.含有大量Fe3+的溶液中:Al3+、Cu2+、Cl-、SO42— |
| C.加入Al能放出H2的溶液中:K+、NH4+、NO3—、Cl- |
| D.水电离的c(H+)=10-12 mol/L的溶液中:K+、Ba2+、NO3—、I- |
B
解析

练习册系列答案
相关题目
某钠盐溶液中可能含有NO2-、SO42-、SO32-、CO32-、Cl-、NO3-等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
①用pH计测得溶液pH大于7
②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体
④加足量BaCl2溶液,产生白色沉淀,该沉淀完全溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色
⑤加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)2溶液,再滴加KSCN溶液,显红色
则下列说法不正确的是
| A.由②中的实验现象可推测一定含有NO2- |
| B.根据②③④可确定一定含有NO2-、CO32-、Cl-三种阴离子 |
| C.不能确定是否一定含有NO3- |
| D.由④即可确定一定不存在SO42-、SO32- |
将足量CO2分别通入下列各溶液中,所含离子仍能大量共存的是( )
| A.NH4+ 、Al3+ 、SO42-、H+ | B.Na+ 、CH3COO- 、C6H5O- 、HCO3- |
| C.Na+、ClO- 、SO42-、Cl- | D.K+、AlO2-、Cl- 、NO3- |
向含等物质的量两种溶质的甲溶液中逐渐加入乙物质,生成不溶物的量(Y)与加入物的量(X)之间的关系符合如图所示的是
| | 甲溶液 | 乙物质 |
| A | HCl和CaCl2 | NaHCO3溶液 |
| B | H2SO4和MgSO4 | NaOH溶液 |
| C | Fe2(SO4)3和CuSO4 | Fe粉 |
| D | AlCl3和HCl | NH3气体 |
某无色溶液含有①Na+、②Ba2+、③Cl-、④Br-、⑤SO32-、⑥SO42-中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
| 步骤 | 操作 | 现象 |
| (1) | 用pH试纸检验 | 溶液的pH大于7 |
| (2) | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈橙色 |
| (3) | 向所得水溶液中加入Ba(NO3)2溶液和稀硝酸 | 有白色沉淀产生 |
| (4) | 过滤,向滤液中加入AgNO3溶液和稀硝酸 | 有白色沉淀产生 |
下列结论正确的是( )
A.肯定含有的离子是①④⑤
B.肯定没有的离子是②⑥
C.不能确定的离子是①
D.不能确定的离子是③⑤
下列解释相关问题或实验的离子方程式不正确的是( )
A.NaClO溶液呈碱性:ClO-+H2O HClO+OH- HClO+OH- |
B.向沸水中滴加饱和FeCl3溶液制胶体:Fe3++3H2O Fe(OH)3(胶体)+3H+ Fe(OH)3(胶体)+3H+ |
| C.粗盐提纯中除去Mg2+:Mg2++2OH-=Mg(OH)2↓ |
| D.工业上精炼粗铜的阴极反应:Cu-2e-=Cu2+ |
能正确表示下列反应的离子方程式的为( )
A.硫化亚铁溶于稀硝酸中:FeS+2H+ Fe2++H2S↑ Fe2++H2S↑ |
B.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O Al Al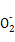 +4N +4N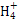 +2H2O +2H2O |
C.硫代硫酸钠溶液中滴入稀盐酸:S2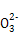 +2H+ +2H+ S↓+SO2↑+H2O S↓+SO2↑+H2O |
D.在NaHSO4溶液中滴加Ba(OH)2至中性:H++S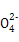 +Ba2++OH- +Ba2++OH- BaSO4↓+H2O BaSO4↓+H2O |
已知电离平衡常数:H2CO3>HClO>HCO3—,氧化性:HClO>Cl2>Br2>Fe3+>I2。下列有关离子反应或离子方程式的叙述中,正确的是( )
| A.向FeI2溶液中滴加少量氯水,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl- |
| B.向溴水中加入足量氯化亚铁溶液能使溴水变成无色 |
| C.向NaClO溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O=2HClO+CO32— |
| D.能使pH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、Br-能大量共存 |
下列离子方程式书写正确的是( )
| A.将铜屑加入Fe3+溶液中:Fe3++Cu=Fe2++Cu2+ |
B.NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH- NH3↑+H2O NH3↑+H2O |
| C.稀硝酸和过量的铁屑反应: Fe+4H++NO3-=Fe3++NO↑+2H2O |
| D.KI溶液与H2SO4酸化的H2O2溶液混合:2I-+H2O2+2H+=I2+2H2O |