题目内容
【题目】NA为阿伏加德罗常数的值。下列有关叙述正确的是( )
A.0.1 mol C2H6O分子中含有C—H键数为0.5NA
B.0.1 mol Cl2和0.1 mol HI充分反应后气体分子数为0.2NA
C.CO2通过Na2O2使其增重2.8 g,反应中转移电子数为0.2NA
D.3.0 g甲醛(HCHO)和乙酸的混合物中含有的原子总数为0.4NA
【答案】D
【解析】
A.0.1molC2H6O,如果为乙醇(CH3CH2OH),则含有C-H键数为0.5NA,如果为甲醚(CH3OCH3),则C-H键数为0.6NA,故A 错误;
B.氯气与碘化氢反应的方程式为Cl2+2HI=I2+2HCl,0.1molCl2和0.1molHI反应,氯气过量,HI完全反应,反应完成后体系中含有0.1molHCl,0.05molCl2,0.05molI2,气体分子数为0.15NA,故B错误;
C.依据方程式:2Na2O2+2CO2=2Na2CO3+O2,固体增加56g,转移2mole-,所以CO2通过Na2O2使其增重2.8g,反应中转移电子数为![]() ×2 NA =0.1NA,故C错误;
×2 NA =0.1NA,故C错误;
D.3.0g含甲醛和乙酸混合物中含有0.1mol最简式CH2O,含有0.4mol原子,含有的原子总数为0.4NA,故D正确;
故选D。

 口算题天天练系列答案
口算题天天练系列答案【题目】如图所示,x、y分别是直流电源的两极,通电后发现a极极板处有无色、无味的气体放出,b极极板质量增加,符合这一情况的是( )
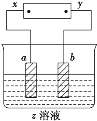
选项 | a极板 | b极板 | x电极 | z溶液 |
A | 锌 | 石墨 | 正极 | CuSO4 |
B | 石墨 | 石墨 | 负极 | NaOH |
C | 石墨 | 银 | 正极 | AgNO3 |
D | 铜 | 石墨 | 负极 | CuCl2 |
A.AB.BC.CD.D
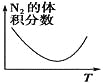
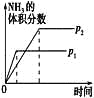
【题目】对于可逆反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0。下列研究目的和图示相符的是
2NH3(g) ΔH<0。下列研究目的和图示相符的是
A | B | C | D | |
研究目的 | 温度(T)对反应的影响(T2>T1) | 压强(p)对平衡常数的影响 | 温度(T)对反应的影响 | 压强(p)对反应的影响(p2>p1) |
图示 |
|
|
|
|
A.AB.B .C.CD.D