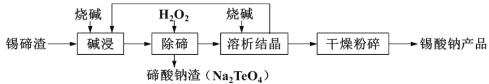
题目内容
【题目】实验室需要配制0.1 mol·L-1 CuSO4溶液480 mL。按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、量筒、玻璃棒、 ________、________以及等质量的两片张滤纸。
(2)计算,应选择下列________。
A.需要CuSO4固体8.0 g B.需要CuSO4·5H2O晶体12.0 g
C.需要CuSO4·5H2O晶体12.5 g D.需要CuSO4固体7.7 g
(3)称量。所用砝码生锈则所配溶液的浓度会________(填“偏高”“偏低”或“无影响”,下同)。
(4)溶解、冷却。若未冷却,则所配溶液浓度会________。
(5)转移、洗涤。若未洗涤,则所配溶液浓度会________。
(6)定容,摇匀。
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,贴好标签,注明配制的时间、溶液名称及浓度。

(8)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会________。
【答案】胶头滴管 500 mL容量瓶 AC 偏高 偏高 偏低 偏低
【解析】
本题是一定量浓度溶液配制题目,注意其操作的相关注意事项即可
(1)配制的是480 mL溶液,需要容量瓶不能小于此体积,又定容后期需要胶头滴管,故本题答案为胶头滴管、500 mL容量瓶;
(2)因为定容时使用的500 mL容量瓶,其物质称量时时按500 mL算,不是按480 mL算,若果是硫酸铜固体其质量为![]() =8.0g,若为5水硫酸铜其质量为
=8.0g,若为5水硫酸铜其质量为![]() =12.5g,故答案为A、C;
=12.5g,故答案为A、C;
(3)砝码生锈,其砝码质量比本身标记质量大,其称量的物质质量增大,其配置容溶液浓度会偏高,故答案为偏高;
(4)若未冷却,会导致定容的溶液体积减少,最终导致溶液浓度偏高,故本题答案为偏高;
(5)若未洗涤,其烧杯中还残留有少量物质,其溶液中溶质质量减少,最终导致溶液浓度偏低,故本题答案为偏低;
(8)因仰视,溶液体积偏大,最终导致溶液浓度偏低,故本题答案为偏低。

【题目】下列有关实验的现象和结论都正确的是
选项 | 实验 | 现象 | 结论 |
A | 测定等浓度的 |
| 非金属性: |
B | 将稀硫酸加入到碳酸钙中,排饱和食盐水收集气体 | 收集到一定量气体 | 实验室可用此法制备 |
C | 将4mL |
| 增大反应物浓度, 反应速率加快 |
D | 将 | 溶液变红 |
|
A.AB.BC.CD.D
【题目】在相同的密闭容器中,用两种不同方法制得的![]() 分别进行催化分解水的实验:
分别进行催化分解水的实验:![]()
![]() ,水蒸气的浓度
,水蒸气的浓度![]() 随时间
随时间![]() 变化如表所示。
变化如表所示。
序号 |
a克 | 温度
| 0 | 10 | 20 | 30 | 40 | 50 |
① | 方法I |
|
|
|
|
|
|
|
② | 方法 |
|
|
|
|
|
|
|
③ | 方法II |
|
|
|
|
|
|
|
下列叙述正确的是
A.实验①前20min的平均反应速率![]()
B.实验①比实验②所用的![]() 催化效率高
催化效率高
C.实验的温度:![]()
D.实验①、②、③的化学平衡常数的关系:![]()
【题目】硫酸锌是一种重要的工业原料,广泛用于农业、化工、电镀等行业。工业上由锌渣(主要成分为ZnO、FeO、CuO、PbO等)等工业废料生产ZnSO4·7H2O的流程如下:
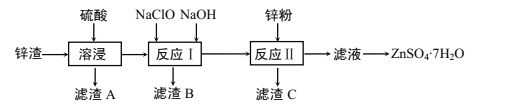
(1)“溶浸”操作中,选用“锌渣”而不选择氧化锌矿粉的原因是______;该操作中不断通入高温水蒸气的目的是________。
(2)“滤渣A”的主要成分是________。
(3)“反应Ⅰ”中,加入NaClO反应的离子方程式为___。
(4)“反应Ⅰ”中,再加入NaOH调节pH约为4.5,则“滤渣B”的主要成分是_____(填化学式)。(Ksp[Zn(OH)2]=3×10-17,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=2.8×10-39)
(5)“反应Ⅱ”中,加入的锌粉需用少量稀硫酸处理,原因是_________。
(6)取28.7gZnSO4·7H2O加热至不同温度,剩余固体的质量如下表:
温度/℃ | 100 | 250 | 680 | 930 |
质量/g | 17.90 | 16.10 | 13.43 | 8.10 |
则680℃时所得固体的化学式为_________(填字母标号)。
A.ZnO B.Zn3O(SO4)2 C.ZnSO4 D.ZnSO4·H2O