题目内容
【题目】我国濒临海域的省份,能够充分利用海水制得多种化工产品。如图是以海水、贝壳(主要成分CaCO3)等为原料制取几种化工产品的工艺流程图,其中E是一种化肥,N是一种常见的金属单质。
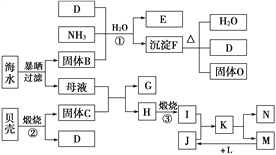
结合上述工艺流程图回答下列问题:
(1)物质G和L的化学式分别为________和________________。
(2)上述工艺流程图中可以循环使用的物质的化学式为______。
(3)反应①的化学方程式为______________________________;在反应①中必须先通入NH3,而后通入D,其原因是____________________。
(4)工业上利用F可制得另一种化工产品,该反应的化学方程式为________________。
(5)由K溶液经如何处理才能制得N?_____________________。
【答案】 CaCl2 H2 CO2 NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl NH3在溶液中的溶解度大,利于吸收CO2,使其转化为NaHCO3 2NaHCO3![]() Na2CO3+CO2↑+H2O MgCl2溶液必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,电解熔融MgCl2可制取金属镁
Na2CO3+CO2↑+H2O MgCl2溶液必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,电解熔融MgCl2可制取金属镁
【解析】题中的工艺流程图由海水晒盐、海水提镁和工业制纯碱三部分组成。分析工艺流程图中的转化关系可得B、C、D、E、F、G、H、I、J、K、L、M、N、O分别是NaCl、CaO、CO2、NH4Cl、NaHCO3、CaCl2、Mg(OH)2、MgO、HCl、MgCl2、H2、Cl2、Mg、Na2CO3。则
(1)根据以上分析可知物质G和L的化学式分别为CaCl2、H2。(2)在用贝壳制生石灰的同时生成CO2,在将NaHCO3加热分解制纯碱时也生成CO2,CO2可循环利用。(3)反应①是用NaCl、NH3、CO2和H2O反应制取NaHCO3和NH4Cl的反应,化学方程式为NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl。NH3在水溶液中的溶解度大,利于吸收较多量的CO2使其转化为NaHCO3。(4)工业上用NaHCO3受热分解可制得纯碱,化学方程式为2NaHCO3![]() Na2CO3+CO2↑+H2O。(5)氯化镁易水解生成氢氧化镁和氯化氢,加热促进水解,因此MgCl2溶液必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,再电解熔融MgCl2可制得金属镁。
Na2CO3+CO2↑+H2O。(5)氯化镁易水解生成氢氧化镁和氯化氢,加热促进水解,因此MgCl2溶液必须在氯化氢气体中进行蒸发结晶制得无水MgCl2,再电解熔融MgCl2可制得金属镁。

【题目】下列实验事实不能用平衡移动原理解释的是( )
A.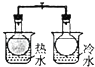 将NO2球浸泡在冷水和热水中
将NO2球浸泡在冷水和热水中
B.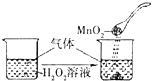 向H2O2溶液中滴加MnO2粉末
向H2O2溶液中滴加MnO2粉末
C.
T(℃) | 25 | 50 | 100 |
水的离子积常数KW(×10﹣14) | 1.01 | 5.47 | 55.0 |
D.
c(氨水)/mol.L﹣1 | 0.1 | 0.01 |
pH | 11.1 | 10.6 |