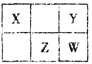题目内容
【题目】如下图所示表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨晶体结构中的某一种的某一部分。

(1)其中代表金刚石的是(填编号字母,下同)________,其中每个碳原子与________个碳原子最接近且距离相等。金刚石属于________晶体。
(2)其中代表石墨的是_______,其中每个正六边形占有碳原子数平均为________个。
(3)其中代表NaCl晶体的是________,每个Na+周围与它最接近且距离相等的Na+有________个。
(4)代表CsCl晶体的是________,它属于________晶体,每个Cs+与________个Cl-紧邻。
(5)代表干冰的是________,它属于________晶体,每个CO2分子与________个CO2分子紧邻。
(6)上述五种物质熔点由高到低的排列顺序为________。
【答案】 D 4 原子 E 2 A 12 C 离子 8 B 分子 12 石墨>金刚石>NaCl>CsCl>干冰
【解析】(1)在金刚石晶胞中,每个碳可与周围4个碳原子形成共价键,将这4个碳原子连结起来后可以形成正四面体,体心有一个碳原子,所以图D为金刚石,每个碳原子与4个碳原子最近且距离相等;金刚石是空间网状结构,属于原子晶体,故答案为:D,4,原子;
(2)石墨是层状结构,在层与层之间以范德华力相互作用,在层内碳与碳以共价键相互作用,形成六边形,所以图E为石墨的结构,每个正六边形占有的碳原子数平均为6×![]() =2;故答案为:E,2;
=2;故答案为:E,2;
(3)在NaCl晶胞中,每个钠离子周围有六个氯离子,每个氯离子周围也有六个钠离子,所以图A为NaCl的结构,根据晶胞的结构,每个钠离子周围距离最近的钠离子在小立方体的面对角线的位置,每个钠离子周围有八个这样的立方体,所以每个钠离子周围与它最近且距离相等的钠离子就有12个;故答案为:A,12;
(4)CsCl的晶胞中铯离子和氯离子的配位数都是8,即每个铯离子周围有8个氯离子,每个氯离子周围也有8个铯离子,所以图C为CsCl的结构,属于离子晶体;故答案为:C,离子;8;
(5)干冰是分子晶体,CO2分子位于立方体的顶点和面心上,以顶点上的CO2分子为例,与它距离最近的CO2分子分布在与该顶点相连的12个面的面心上,所以图B为干冰晶体;故答案为:B,分子;12;
(6)各种物质的熔点:原子晶体>离子晶体>分子晶体,石墨的熔点大于金刚石,在离子晶体里,半径越大,晶格能越小,熔点越低,由于铯离子半径大于钠离子,石墨的熔点大于金刚石,所以熔点由高到低的排列顺序为:石墨>金刚石>NaCl>CsCl>干冰;故答案为:石墨>金刚石>NaCl>CsCl>干冰。

【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)元素p为26号元素,请写出其原子的三价阳离子的电子排布式:______________。
(2)e与a反应的产物的分子中中心原子的杂化形式为__________,该分子是__________(填“极性”或“非极性”)分子。
(3)请写出f的氢化物在水中所存在氢键的表达式:(任写两种即可)_________________________。
(4)o、p两元素的部分电离能数据列于下表:
元素 | o | p | |
电离能 /kJ·mol-1 | I1 | 717 | 759 |
I2 | 1 509 | 1 561 | |
I3 | 3 248 | 2 957 | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是___________________________________;
(5)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

请问晶胞中i原子的配位数为________,一个晶胞中i原子的数目为________。