题目内容
【题目】元素及其化合物在生活及生产中有很多重要用途。
Ⅰ.SiC、BN、GaAs 等是人工合成半导体的材料,具有高温、高频、大功率和抗辐射等优点。请回答:
(1)第一电离能:Ga_______As(填“>”、 “<”、“=”)。
(2)B、C、N的电负性由小到大排列为_______
Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)拟卤素(CN)2、(SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足 8 电子结构。(SCN)2对应的酸有两种,测得硫氰酸(H—S—C≡N )的沸点低于异硫氰酸(H—N=C=S),其原因是_______。
(2)卤化物 RbICl2在加热时会分解为晶格能相对较大的卤化物 A 和卤素互化物或卤素单质,A 的化学式为_______;I3+属于多卤素阳离子,其空间构型为_______
(3)卤素互化物如IBr、ICl等与卤素单质结构和性质相似。Cl2、IBr、ICl沸点由高到低的顺序为_______。
(4)请推测①HC1O4、②HIO4、③H5IO6[可写成(HO)5IO]三种物质的酸性由强到弱的顺序为_______(填序号)。
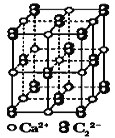
(5)CaC2晶体的晶胞结构与 NaCl 晶体的相似(如图所示),CaC2晶体中的哑铃形 C22﹣的存在,使晶胞沿一个方向拉长。此晶体中 1 个 C22﹣周围距离最近的Ca2+为_______个;若该晶胞的边长为a、a、b(pm),则该晶体的密度为_______g·cm-3(写出表达式)。
【答案】<B<C<N异硫氰酸中存在分子间氢键,而硫氰酸中无氢键RbClV形IBr>ICl>Cl2①>②>③4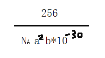
【解析】
Ⅰ.由同周期自左而右,第一电离能增大,电负性增大可知第一电离能:Ga小于As;B、C、N的电负性依次增大,故答案为< 、B<C<N;Ⅱ.(1)因在异硫氰酸分子中存在H-N键,故其分子间存在氢键,导致其沸点较高,故答案为异硫氰酸中存在分子间氢键,而硫氰酸中无氢键;(2)RbICl2加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,氯离子的半径小于碘离子的半径,则RbCl的离子键长小于RbI的离子键长,则RbCl的晶格能较大,则A为RbCl,I3+的成键数为2,孤对电子数为(7-1-2×1)÷2=2,与水相似,则空间构型为V形,故答案为:RbCl、V形;(3)一般结构相似的分子晶体,相对分子质量越大,沸点越高,则沸点为BrI>ICl>Cl2,故答案为BrI>ICl>Cl2;(4)一般含氧酸中含非羟基氧原子个数越多,酸性越强,①HC1O4、②HIO4、③H5IO6中的非羟基氧分别为3、3、1,但非金属性Cl>I,则酸性为①②③,故答案为:①>②>③;(5)依据晶胞示意图可以看出,晶胞的一个平面的长与宽不相等,再由图中体心可知1 个 C22﹣周围距离最近的Ca2+为4个,而不是6个;根据均摊法可知每个晶胞中含Ca2+为(1+12÷4)=4个,含C22-为(8÷8+6÷2)=4个,则每个晶胞的质量为(4×64÷NA)g,体积为(a2b)pm3=(10-36a2b)m3=(10-30 a2b)cm3,故晶体的密度为![]() g·cm-3。
g·cm-3。