题目内容
【题目】已知X、Y、Z都是金属,若把X浸入Z的盐溶液中,X的表面有Z析出;若X、Y和盐酸溶液形成原电池,Y为电池的负极。则X、Y、Z的金属活动顺序为( )
A. Y>X>Z B. X>Z>Y C. X>Y>Z D. Y>Z>X
【答案】A
【解析】活泼性强的金属可以把活泼性弱的金属从其盐中置换出来,一般情况下原电池中,负极金属的活泼性强于正极金属的活泼性。
把X浸入Z的盐溶液中,X的表面有Z析出,说明金属X可以把金属Z从其盐中置换出来,所以活泼性X>Z;X和Y组成原电池时,Y为电池的负极,所以活泼性Y>X,因此X、Y、Z三种金属的活动性顺序为Y>X>Z。
答案选A。

 阅读快车系列答案
阅读快车系列答案【题目】钴(Co)及其化合物在工业上有广泛应用。利用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO等)制取CoC12·6H2O粗品的工艺流程图如下:
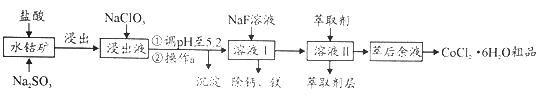
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、A13+等;
②部分阳离子以氢氧化物形式开始沉淀和完全沉淀时的pH如下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
请回答下列问题:
(1)上述工艺流程图中操作a的名称:_______________。
(2)写出“浸出”时Co2O3发生反应的离子方程式:____________________。
(3)加入NaC1O3的作用是________________ 。
(4)萃取剂对金属离子的萃取率与pH的关系如图。使用萃取剂最适宜的pH范围是_________(填字母序号)。
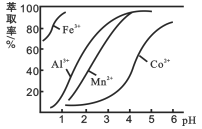
A.2.0~2.5 B. 3.0~3.5 C. 5.0~5.5 D. 9.5~9.8
(5)“除钙”“镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知某温度下,Ksp(MgF2)=7.35×10-11, Ksp(CaF2)=1.50×10-10。当加入过量NaF,所得滤液中c(Mg2+)/c(Ca2+)=_______________。