��Ŀ����
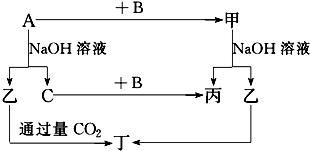
����Ŀ���������õ���ͨ���Ũ��NaOH��H2O2�Ļ��Һ�У��ڵ��ܿ�����Һ�ĽӴ�������˸�ĺ����֣�������Ϊͨ������Һ�в�����ClO����H2O2��ԭ���������ҷ�Ӧ�����������ϸߵ������ӣ�Ȼ������ת��Ϊ��ͨ�����ӣ�����������Ժ��ų�����ʵ�����õ�������������ͼ1��ʾ�� 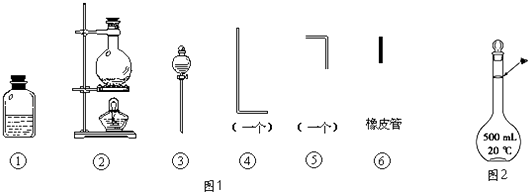
����Ҫ����д���пհף�
��1����װ��������װ��ʱ��Ӧѡ�õ�����������Ϊ����дͼ�б�ţ���
��2����ʵ�����ʱ����������������ҵ�˳�����������ĸ����������ܵı������Ϊ ��
��3�������ٵ���Ƥ��������Ӧ��2����ԭ���� ��
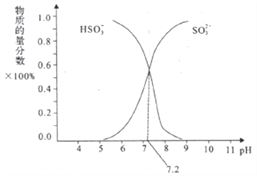
��4����ʵ��������10molL��1��NaOH��Һ500mL���õ�����������������ƽ���ձ��⣬�����õ��������������������ƣ�������ʱ������ͼ2����������ҺŨ�����ƫ�ߡ���ƫ�͡�����
��5��ʵ��ʱ��������ClO����H2O2��Ӧ�����ӷ���ʽΪ ��
���𰸡�
��1���ۢڢ�
��2���ڢݢޢܢ�
��3��ʹƿ����ѹǿ���
��4��500mL����ƿ������������ͷ�ιܣ�ƫ��
��5��ClO��+H2O2=Cl��+O2��+H2O
���������⣺��1�����ڷ�Ӧ���Ƕ������̺�Ũ���ᣬ�����ڷ�Ӧǰ���߲��ܻ�ϣ��÷�Һ©����װŨ���ᣬ��Ҫ�ڢ�װ�ã���Ӧ�����Ǽ��ȣ���Ҫ�ڢڸ�װ�ã�����Ҫ�õ��ܵ��������������õ��ݣ�
���Դ��ǣ��ۢڢݣ���2���ڢ��еij������ǽ���������������ڢٸ�װ�õģ�������Ҫ����Ƥ�ܽ���������̵��������������������������ĸ����������ܵı�������Ǣڢݢޢܢ٣�
���Դ��ǣ��ڢݢޢܢ٣���3������ƿ�ڲ�����������ʹƿ��ѹǿ����������Ƥ���Ŀ�������ը����С����Ϊ��ʹƿ����ѹǿ��ȣ�
���Դ��ǣ�ʹƿ����ѹǿ��ȣ���4������10molL��1��NaOH��Һ500mL����������Ϊ500mL����ƿ������������ͷ�ιܣ�����ʱ����ˮ��ˮƫ�٣���Һ���ƫС����c= ![]() ��֪��Ũ��ƫ�ߣ�
��֪��Ũ��ƫ�ߣ�
���Դ��ǣ�500mL����ƿ������������ͷ�ιܣ�ƫ�ߣ���6���������������ǿ�����ԣ�˫��ˮ�л�ԭ�ԣ����Դ���������Ӻ�˫��ˮ����������ԭ��Ӧ���������ӡ�������ˮ���������ӷ���ʽΪClO��+H2O2=Cl��+O2��+H2O�����Դ��ǣ�ClO��+H2O2=Cl��+O2��+H2O��
�����㾫����������Ҫ�����������Ļ�ѧ���ʺ�������ʵ�����Ʒ������֪ʶ�㣬��Ҫ���������Ļ�ѧ���ʣ��������Ӧ�����������ɸ�̬���ǽ�����Ӧ����ˮ��Ӧ����Ӧ���뻹ԭ�����ʷ�Ӧ��ʵ�����Ʒ���MnO2+4HCl��Ũ��=MnCl2+Cl2��+2H2O������ȷ�����⣮