题目内容
【题目】五氧化二钒(V2O5)是重要的催化剂,可用某钒矿石(含有 V2O3、Fe、Al2O3等)来制备,工艺流程如下:
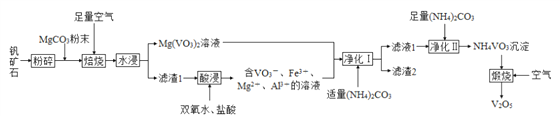
请回答下列问题:
(1) 钒矿石“粉碎”的目的为__________。
(2)“滤渣1” 中除 Al2O3、 Fe(VO3)2、 Fe(VO3)3外,还含有__________(填化学式)。
(3)“酸浸”时,若用硝酸代替双氧水和盐酸,弊端为__________。
(4)“滤渣 2” 的主要成分为 MgCO3、Fe(OH)3和 Al(OH)3,其中生成 Al(OH)3的离子方程式为__________。
(5) 若“净化Ⅰ” 时直接加入足量的(NH4)2CO3,可能导致的后果为__________。
(6)“煅烧”时,还生成参与大气循环的气体,该反应的化学方程式为__________。
(7)产品中 V2O5纯度的测定: 称取产品 a g, 先用硫酸溶解,得到(VO2)2SO4溶液;再加入 V1 mL c1 mol·L-1 (NH4)2Fe(SO4)2溶液(VO2++2H++Fe2+=VO2++Fe3++H2O); 最后用 c2 mol·L-1 KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗 KMnO4标准溶液的平均体积为 V2 mL。假设杂质不参与反应,则产品中 V2O5的质量分数为__________%。
【答案】 增大钒矿石的比表面积,加快焙烧速率, 使焙烧充分 MgO 生成氮的氧化物等有毒气体,污染环境 2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑ 生成 NH4VO3沉淀, 使钒的利用率降低 4NH4VO3+3O2 ![]() 2V2O5+2N2+8H2O
2V2O5+2N2+8H2O ![]()
【解析】(1) 钒矿石“粉碎”增大反应物的接触面积,加快反应速率,即目的为增大钒矿石的比表面积,加快焙烧速率,使焙烧充分。(2)碳酸镁高温下易分解生成氧化镁和CO2,所以“滤渣1” 中除 Al2O3、Fe(VO3)2、Fe(VO3)3外,还含有MgO。(3)“酸浸”时,若用硝酸代替双氧水和盐酸,硝酸钡还原为氮的氧化物,因此弊端为生成氮的氧化物等有毒气体,污染环境。(4)溶液中铝离子和碳酸根水解相互促进生成氢氧化铝,因此其中生成 Al(OH)3的离子方程式为2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑。(5) 若“净化Ⅰ” 时直接加入足量的(NH4)2CO3会生成NH4VO3沉淀,从而使钒的利用率降低。(6)“煅烧”时,还生成参与大气循环的气体,该气体是氮气,反应的化学方程式为4NH4VO3+3O2 ![]() 2V2O5+2N2+8H2O。(7)根据电子得失守恒可知剩余亚铁离子的物质的量是0.001V2c2mol×5,因此参与反应VO2++2H++Fe2+=VO2++Fe3++H2O的亚铁离子是0.001V1c1mol-0.001V2c2mol×5,所以V原子的物质的量是0.001V1c1mol-0.001V2c2mol×5,则根据V原子守恒可知产品中V2O5的质量分数为
2V2O5+2N2+8H2O。(7)根据电子得失守恒可知剩余亚铁离子的物质的量是0.001V2c2mol×5,因此参与反应VO2++2H++Fe2+=VO2++Fe3++H2O的亚铁离子是0.001V1c1mol-0.001V2c2mol×5,所以V原子的物质的量是0.001V1c1mol-0.001V2c2mol×5,则根据V原子守恒可知产品中V2O5的质量分数为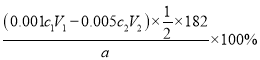 =
=![]() 。
。

 阅读快车系列答案
阅读快车系列答案