题目内容
【题目】已知HA的酸性比HB弱,在物质的量浓度均为0.1mol·L-1的NaA和NaB混合溶液中,下列排序正确的是( )
A.c(OH-)>c(HA)>c(HB)>c(H+)
B.c(OH-)>c(A-)>c(B-)>c(H+)
C.c(OH-)>c(B-)>c(A-)>c(H+)
D.c(OH-)>c(HB)>c(HA)>c(H+)
【答案】A
【解析】
在NaA溶液中:A-+H2O![]() HA+OH-,H2O
HA+OH-,H2O![]() H++OH-;在NaB溶液中:B-+H2O
H++OH-;在NaB溶液中:B-+H2O![]() HB+OH-,H2O
HB+OH-,H2O![]() H++OH-,则c(A-)>c(OH-)>c(HA)>c(H+),c(B-)>c(OH-)>c(HB)>c(H+)。
H++OH-,则c(A-)>c(OH-)>c(HA)>c(H+),c(B-)>c(OH-)>c(HB)>c(H+)。
A.已知HA的酸性比HB弱,则0.1mol·L-1的NaA和NaB混合溶液中,A- 水解的程度比B- 大,c(HA)>c(HB),从而得出c(OH-)>c(HA)>c(HB)>c(H+),A正确;
B.HA的酸性比HB弱,则A- 水解的程度比B- 大,所以c(A-)<c(B-),B不正确;
C.盐类单水解的程度都不大,也就是剩余量大于水解消耗量,所以c(H+)<c(OH-)<c(A-)<c(B-),C不正确;
D.由A中分析知,NaA和NaB混合溶液中,c(OH-)>c(HA)>c(HB) >c(H+),D不正确;
故选A。

【题目】计算机记忆材料生产中产生大量的钌废料,一种从钌废料[含Ru(OH)3、FeO、MnO、SiO2及少量的Au]中合成六氯钌酸铵[(NH4)2RuCl6]的流程如下:
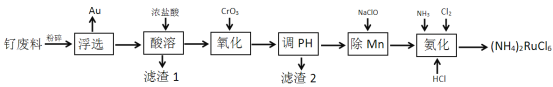
回答下列问题
(1)(NH4)2RuCl6中Ru的化合价为___________。
(2)滤渣1的成分是________ 。
(3)加入CrO3发生反应的离子方程式为______________ 。
(4)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如下表,调pH时,应调整的pH范围为_________。
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.8 | 3.2 |
Cr3+ | 4.6 | 5.9 |
Fe2+ | 5.8 | 11.2 |
Mn2+ | 8.8 | 10.9 |
Ru3+ | 7.9 | 11.3 |
(5)加入NaClO后,Mn以MnO2的形式沉淀而除去,该反应中氧化剂与还原剂的物质的量之比为________。
(6)氨化时发生反应的化学方程式为____________
(7)氨化时,投料比![]() 对(NH4)2RuCl6产率的影响如图所示:
对(NH4)2RuCl6产率的影响如图所示:
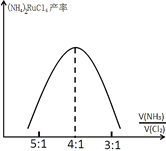
(NH4)2RuCl6的产率在![]() 为4:1后降低,其原因可能是_______________。
为4:1后降低,其原因可能是_______________。
(8)已知钌废料中钌含量为53%,氨化时产率为91%,其余步骤损失率合计为11%,则2吨钌废料可制得(NH4)2RuCl6________Kg。