题目内容
下列中学常见实验的现象或表述正确的是( )
| A、在酒精灯上灼烧用砂纸打磨过的铝箔(已除氧化膜),会发现熔化的铝不断滴落 |
| B、向盛有沸水的烧杯中滴加FeCl3溶液并长时间煮沸,制备Fe(OH)3胶体 |
| C、铁和镁均是较活泼的金属,易被空气中的氧气氧化而形成一层致密的氧化膜 |
| D、铁和高温水蒸气的实验中,可用干净的细铁丝代替还原铁粉进行实验 |
考点:铝的化学性质,镁的化学性质,铁的化学性质
专题:元素及其化合物
分析:A.铝箔在空气中被氧化为氧化铝,加热时,表面的氧化铝的熔点比铝的熔点高,包住了里边熔化的铝,所以加热铝箔的时候铝熔化了但是不会滴落;
B.实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色.如果长时间煮沸将得到氢氧化铁沉淀;
C.活泼金属镁在空气中易与氧气反应,在表面生成一层致密的氧化膜,可以保护内层金属不被继续氧化,铁不能;
D.在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应,可用干净的细铁丝代替还原铁粉进行实验;
B.实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色.如果长时间煮沸将得到氢氧化铁沉淀;
C.活泼金属镁在空气中易与氧气反应,在表面生成一层致密的氧化膜,可以保护内层金属不被继续氧化,铁不能;
D.在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应,可用干净的细铁丝代替还原铁粉进行实验;
解答:
解:A.将铝箔用坩埚钳夹住放在酒精灯火焰上加热,铝和氧气反应生成了氧化铝,又因三氧化二铝的熔点高于铝的熔点,而三氧化二铝在铝的表面,所以加热铝箔的时候铝失去了光泽,铝熔化了但是不会滴落,故A错误;
B.制备氢氧化铁胶体时,当溶液呈红褐色时应停止加热,否则生成的胶体在加热条件下发生聚沉,形成红褐色沉淀,故B错误;
C.根据金属的性质,活泼金属镁在空气中易与氧气反应,在表面生成一层致密的氧化膜氧化镁(氧化镁),该氧化膜可以保护内层金属不被继续氧化,而铁属于较活泼的金属,在空气中易生锈,且不能在表面生成一层致密的氧化膜,故C错误;
D.铁和高温水蒸气反应化学方程式为:3Fe+4H2O(g)
Fe3O4+4H2↑,铁粉与细铁丝相比,接触面积大,该实验可用干净的细铁丝代替还原铁粉进行实验,几乎不影响实验结果,故D正确;
故选D.
B.制备氢氧化铁胶体时,当溶液呈红褐色时应停止加热,否则生成的胶体在加热条件下发生聚沉,形成红褐色沉淀,故B错误;
C.根据金属的性质,活泼金属镁在空气中易与氧气反应,在表面生成一层致密的氧化膜氧化镁(氧化镁),该氧化膜可以保护内层金属不被继续氧化,而铁属于较活泼的金属,在空气中易生锈,且不能在表面生成一层致密的氧化膜,故C错误;
D.铁和高温水蒸气反应化学方程式为:3Fe+4H2O(g)
| ||
故选D.
点评:本题考查有关元素化合物方面的实验知识,题目难度不大,掌握钠、镁、铁的性质是解答本题的关键,注意实验方法制备氢氧化铁胶体为高频考点.

练习册系列答案
 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
下列操作达不到预期目的是( )
①石油分馏时把温度计水银球插入受热的液体中;
②用酸性高锰酸钾溶液除去乙炔中含有的H2S;
③用溴乙烷在NaOH溶液中加热后,加入AgNO3溶液检验卤素原子;
④将苯和溴水混合后加入铁粉制取溴苯;
⑤将敞口久置的电石与蒸馏水混合制取乙炔.
①石油分馏时把温度计水银球插入受热的液体中;
②用酸性高锰酸钾溶液除去乙炔中含有的H2S;
③用溴乙烷在NaOH溶液中加热后,加入AgNO3溶液检验卤素原子;
④将苯和溴水混合后加入铁粉制取溴苯;
⑤将敞口久置的电石与蒸馏水混合制取乙炔.
| A、①⑤ | B、③④⑤ |
| C、①②③⑤ | D、①②③④⑤ |
下列说法正确的是( )
| A、HCHO溶液、(NH4)2SO4溶液均能使蛋白质变性 |
| B、煤的干馏是物理变化,煤的气化和液化是化学变化 |
| C、纤维素、蛋白质、油脂均为天然高分子化合物 |
D、聚碳酸酯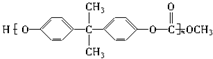 中含有 中含有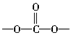 结构 结构 |
把质量为m g的铜丝灼烧变黑,立即放入下列物质中,使铜丝变红,而且质量仍为m g的是( )
①稀硫酸 ②C2H5OH ③稀硝酸 ④CO.
①稀硫酸 ②C2H5OH ③稀硝酸 ④CO.
| A、①② | B、②④ | C、③④ | D、②③ |
有关氧化还原反应的叙述正确的是( )
| A、物质所含元素化合价升高的反应是还原反应 |
| B、氧化还原反应的实质是有氧元素的得失 |
| C、氧化还原反应的实质是元素化合价的升降 |
| D、有单质参加或生成的化学反应不一定是氧化还原反应 |
Ag2Se单晶呈六角微型管状,有望开发为新型材料,其制取原理为:4AgCl+3Se+6NaOH═2Ag2Se+Na2SeO3+4NaCl+3H2O关于该反应下列叙述正确的是( )
| A、AgCl作氧化剂 |
| B、6mol NaOH参加反应转移6mol e- |
| C、氧化剂与还原剂的质量比为1:2 |
| D、被还原的元素与被氧化的元素的物质的量之比为2:1 |