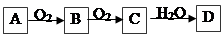题目内容
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | ⑦ | | | ⑧ | |
(2)②、⑧、⑦的最高价含氧酸的酸性由强到弱的顺序是【用化学式表示】 。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: 。
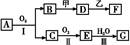
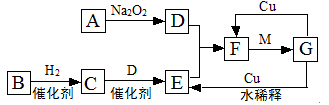
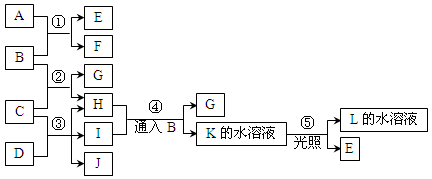
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为 ,N→⑥的单质的化学方程式为 。
(1)O2-> Na+ > Al3+ (2)HClO4>H2CO3>H2SiO3(H4SiO4)
(3) 或
或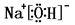
(4)Al3++3NH3·H2O = Al(OH)3↓+3 NH4+ 
解析试题分析:根据元素在周期表中的分布,可以知道①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是Cl;(1)④、⑤、⑥的离子为O2-、 Na+、 Al3+,三者电子层结构相同,根据微粒半径比较原则:电子层结构相同的微粒,核电荷数越大半径越小,则离子半径: O2-> Na+ > Al3+;(2)根据同周期同主族元素性质递变规律知,②、⑧、⑦的最高价含氧酸的酸性由强到弱的顺序是HClO4>H2CO3>H2SiO3(H4SiO4) ;(3)①④⑤⑧分别是H、O、Na、Cl,其中钠元素、氧原子、氢元素组成的氢氧化钠,钠元素、氧原子、氯元素组成的次氯酸钠,均是既含离子键又含极性共价键的化合物,电子式为: 或
或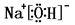
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生如图转化的反应,其中M是仅含非金属的盐,所以一定是铵盐;结合转化关系:Z→⑥的单质铝,逆推N是氧化铝,Z是氢氧化铝,分析产物结合反应:X+Y+H2O→Al(OH)3+NH4+ 可知X与Y的反应是铝盐和一水合氨的反应;离子方程式为:Al3++3NH3·H2O = Al(OH)3↓+3 NH4+,N→⑥的单质的化学方程式为
考点:考查元素周期表的结构、元素位置、规律变化的应用及相关元素化合物知识。

练习册系列答案
相关题目