题目内容
【题目】根据下列有关图象,说法正确的是( )
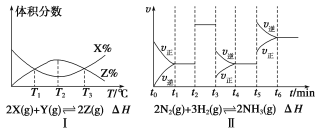

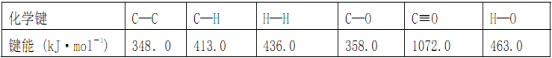
①由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的ΔH<0
②由图Ⅱ知,反应在t6时刻,NH3体积分数最大
③由图Ⅱ知,t3时采取减小反应体系压强的措施
④图Ⅲ表示在10 L容器、850 ℃时的反应,由图知,到4 min 时,反应放出51.6 kJ的热量
A.①③ B.②④ C.③④ D.②③
【答案】C
【解析】
试题分析:①由图Ⅰ知,反应在T1、T3处反应物和生成物的体积分数相对但反应不一定达到平衡,T2-T3升高温度,反应物体积分数增大,生成物体积分数减小,平衡向逆反应方向移动,所以正反应是放热反应,△H<0,故①错误;②由图Ⅱ知,t2时刻正逆反应速率都增大且相等,改变的条件是加入催化剂,平衡不移动;t3时刻正逆反应速率都减小,且逆反应速率大于正反应速率,改变的条件是减小压强,平衡向逆反应方向移动;t5时刻正逆反应速率都增大,且逆反应速率大于正反应速率,改变的条件是升高温度,平衡向逆反应方向移动,所以反应在t1时,NH3体积分数最大,故②错误;③由图Ⅱ知,t3时刻正逆反应速率都减小,且逆反应速率大于正反应速率,改变的条件是减小压强,故③正确;④该反应是一个放热反应,1molCO完全转化时放出43KJ能量,当转化(0.30-0.18)mol/L×10L=1.2molCO时放出51.6kJ的热量,故④正确;故选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目