题目内容
下列①~⑨是元素周期表的前三周期中的部分元素,请从这些元素中选择填空:
(1)上述元素中,化学性质最稳定的是:
(2)⑥和⑦两种元素的最高价氧化物对应的水化物都是碱,则这两种碱的碱性强弱为:NaOH
(3)元素③和元素⑤形成的氢化物中,稳定性较强的是:
(4)画出元素②的原子结构示意图: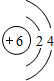
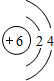 ;
;
(5)元素①和元素⑧的单质均为气态,两气体在一定条件下反应之后的产物可溶于蒸馏水,此水溶液呈
族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
Ar
Ar
(填元素符号);(2)⑥和⑦两种元素的最高价氧化物对应的水化物都是碱,则这两种碱的碱性强弱为:NaOH
>
>
Mg(OH)2(填“>”、“<”或“=”);(3)元素③和元素⑤形成的氢化物中,稳定性较强的是:
HF
HF
(填化学式);(4)画出元素②的原子结构示意图:
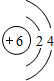
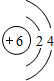
(5)元素①和元素⑧的单质均为气态,两气体在一定条件下反应之后的产物可溶于蒸馏水,此水溶液呈
酸
酸
性(填“酸”、“碱”或“中”).分析:由元素在周期表中的位置可知,①是H、②是C、③是N、④是O、⑤是F、⑥是Na、⑦是Mg、⑧是Cl、⑨是Ar;
(1)稀有气体的化学性质最稳定;
(2)根据金属性越强最高价氧化物对应的水化物碱性越强解答,同周期自左而右,金属性减弱;
(3)根据非金属性越强氢化物越稳定解答,同周期自左而右,非金属性增强;
(4)碳原子核外电子数是6,有2个电子层,最外层电子数是4;
(5)氢气与氯气反应生成氯化氢,氯化氢溶于水电离出氢离子.
(1)稀有气体的化学性质最稳定;
(2)根据金属性越强最高价氧化物对应的水化物碱性越强解答,同周期自左而右,金属性减弱;
(3)根据非金属性越强氢化物越稳定解答,同周期自左而右,非金属性增强;
(4)碳原子核外电子数是6,有2个电子层,最外层电子数是4;
(5)氢气与氯气反应生成氯化氢,氯化氢溶于水电离出氢离子.
解答:解:由元素在周期表中的位置可知,①是H、②是C、③是N、④是O、⑤是F、⑥是Na、⑦是Mg、⑧是Cl、⑨是Ar;
(1)Ar是稀有气体,化学性质最稳定,故答案为:Ar;
(2)同周期自左而右,金属性减弱,故金属性Na>Mg,金属性越强最高价氧化物对应的水化物碱性越强,故碱性NaOH>Mg(OH)2,故答案为:>;
(3)同周期自左而右,非金属性增强,故非金属性F>N,非金属性越强氢化物越稳定,故稳定性HF>NH3,故答案为:HF;
(4)碳原子核外电子数是6,有2个电子层,最外层电子数是4,原子结构示意图为: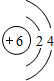 ,故答案为:
,故答案为: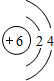 ;
;
(5)氢气与氯气反应生成氯化氢,氯化氢溶于水电离出氢离子,溶液呈酸性,故答案为:酸.
(1)Ar是稀有气体,化学性质最稳定,故答案为:Ar;
(2)同周期自左而右,金属性减弱,故金属性Na>Mg,金属性越强最高价氧化物对应的水化物碱性越强,故碱性NaOH>Mg(OH)2,故答案为:>;
(3)同周期自左而右,非金属性增强,故非金属性F>N,非金属性越强氢化物越稳定,故稳定性HF>NH3,故答案为:HF;
(4)碳原子核外电子数是6,有2个电子层,最外层电子数是4,原子结构示意图为:
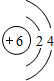 ,故答案为:
,故答案为: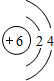 ;
;(5)氢气与氯气反应生成氯化氢,氯化氢溶于水电离出氢离子,溶液呈酸性,故答案为:酸.
点评:本题考查元素周期表、常用化学用语书写、元素周期律等,比较基础,注意基础知识的掌握.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
四种短周期元素的性质或结构信息如下表。下列推断错误的是
| 元素编号 | 元素性质或结构 |
| T | M层上有2对成对电子 |
| X | 元素最高正价是+7价 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | 单质是银白色固体、导电、密度比水小,与水剧烈反应、和氧气反应不同条件下产物不同 |
B.X的最高价氧化物对应的水化物,是无机含氧酸中的最强酸
C.离子半径从小到大的顺序:Y<Z< T < X
D.X、Y形成化合物的晶体类型与X、Z形成化合物的晶体类型不同
下表为部分短周期元素的原子半径及主要化合价,根据表中信息判断,下列叙述正确的是
| 元素代号 | X | Y | Z | M | N |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -1 |
B.最高价氧化物对应的水化物的酸性: H2ZO4>HNO4
C.气态氢化物的稳定性:HM<H2Z
D.M、N形成的简单离子的还原性:N->M-
已知X、Y是主族元素,下表中I为电离能,单位是kJ/mol。下列判断错误的是
|
元素 |
I1 |
I2 |
I3 |
I4 |
|
X |
500 |
4600 |
6900 |
9500 |
|
Y |
580 |
1800 |
2700 |
11600 |
A.元素X的常见化合价是+1价
B.元素Y是ⅢA族的元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第3周期,它可与冷水剧烈反应
 .
.