题目内容
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是

- A.第一电离能和电负性: Z>W>Q
- B.元素W的最高价氧化物对应的水化物的酸性比Q的强
- C.离子半径X3-<Z 3+
- D.元素X与元素Q二者的氢化物能化合生成离子化合物
D
试题分析:根据元素在周期表中的相对位置可知,X是N、Y和O、Z是Al、W是S、Q是Cl。非金属性越强,电负性越大,所以第一电离能和电负性应该是Q>W>Z,A错误;氯元素的非金属性强于S因素的,所以高氯酸的酸性强于氯元素的,B错误;核外电子排布相同的微粒,其离子半径随原子序数的增大而减小,C不正确,离子半径应该是X3->Z 3+。氨气和氯化氢反应生成氯化铵,是离子化合物,D正确,答案选D。
考点:考查元素周期表的结构以及元素周期律的应用和判断
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
试题分析:根据元素在周期表中的相对位置可知,X是N、Y和O、Z是Al、W是S、Q是Cl。非金属性越强,电负性越大,所以第一电离能和电负性应该是Q>W>Z,A错误;氯元素的非金属性强于S因素的,所以高氯酸的酸性强于氯元素的,B错误;核外电子排布相同的微粒,其离子半径随原子序数的增大而减小,C不正确,离子半径应该是X3->Z 3+。氨气和氯化氢反应生成氯化铵,是离子化合物,D正确,答案选D。
考点:考查元素周期表的结构以及元素周期律的应用和判断
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。

练习册系列答案
相关题目
碱金属元素可形成离子型氢化物,下表是同一短周期元素X、Y、Z三种元素氢化物的某些性质
则这三种元素的原子序数从大到小的排列顺序为( )
| 元素 | 熔点(℃) | 沸点(℃) | 与水作用 | 纯液体的导电性 |
| X | -183 | -162 | 不与水反应也不溶于水 | 不导电 |
| Y | -102 | 19 | 放热,形成的酸是弱酸 | 不导电 |
| Z | 680 | - | 剧烈反应生成H2,溶液呈碱性 | 导电 |
| A、X、Y、Z |
| B、Z、X、Y |
| C、Y、X、Z |
| D、Z、Y、X |
短周期元素X、Y、Z、M、R在周期表中的相对位置如图所示.下列说法中不正确的是( )
| X | Y | ||||
| Z | M | R | |||
| A、元素X和Y可以形成两种以上的气态化合物 |
| B、原子半径的大小顺序为:r(Z)>r(M)>r(R) |
| C、元素的最高价氧化物对应水化物的酸性R强于M |
| D、加热蒸干由元素R和Z形成的化合物的水溶液可以得到该化合物的晶体 |
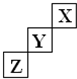 短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法正确的是( )
短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法正确的是( )