题目内容
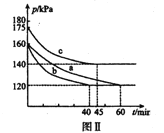
【题目】烧杯中盛有100 mL 1 mol/L的NaHSO4溶液,向其中逐滴滴加1 mol/L的Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图。下列说法中正确的是( )

A. 曲线a表示Na+的物质的量的变化
B. 曲线c表示Ba2+的物质的量的变化
C. 加入50 mL Ba(OH)2溶液时反应的离子方程式为Ba2++2OH-+2H++ ![]() BaSO4↓+2H2O
BaSO4↓+2H2O
D. 加入Ba(OH)2溶液体积大于50 mL后,反应的离子方程式为OH-+H+H2O
【答案】C
【解析】100 mL 1 mol/L的NaHSO4溶液中逐滴滴加1 mol/L的Ba(OH)2溶液,Na+的物质的量不变,故A错误;100 mL 1 mol/L的NaHSO4溶液中滴加100 mL 1 mol/L的Ba(OH)2溶液时, ![]() 恰好沉淀完全,溶液中Ba2+的物质的量为0,故B错误;加入50 mL Ba(OH)2溶液时生成水和硫酸钡的物质的量比为2:1,反应的离子方程式为Ba2++2OH-+2H++
恰好沉淀完全,溶液中Ba2+的物质的量为0,故B错误;加入50 mL Ba(OH)2溶液时生成水和硫酸钡的物质的量比为2:1,反应的离子方程式为Ba2++2OH-+2H++ ![]() BaSO4↓+2H2O,故C正确;加入Ba(OH)2溶液体积等于50 mL时,溶液中的溶质是硫酸钠,再加入Ba(OH)2溶液,反应的离子方程式为Ba2++
BaSO4↓+2H2O,故C正确;加入Ba(OH)2溶液体积等于50 mL时,溶液中的溶质是硫酸钠,再加入Ba(OH)2溶液,反应的离子方程式为Ba2++ ![]() BaSO4↓,故D错误。
BaSO4↓,故D错误。

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目