题目内容
【题目】有四种物质:①氧化铁 ②硫酸 ③碳酸氢钠 ④氢氧化钠
(1)属于盐的是________(填序号),写出这种物质在水溶液中的电离方程式__________。
(2)上述物质中有一种与其他三种物质均能反应,此物质是_________(填序号)。
(3)写出铝与稀硫酸反应的离子方程式,并用双线桥标出电子转移情况________。
【答案】 ③ ![]() ②
② 
【解析】试题分析:本题考查酸、碱、盐、氧化物的概念及相互转化,电离方程式的书写,离子方程式的书写,双线桥标电子转移。
(1)①氧化铁属于氧化物,②硫酸属于酸,③碳酸氢钠属于盐,④氢氧化钠属于碱,属于盐的是③。NaHCO3属于弱酸的酸式盐,在水溶液中的电离方程式为NaHCO3=Na++HCO3-。
(2)四种物质中相互间能发生的反应有:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O、H2SO4+2NaHCO3=Na2SO4+2H2O+2CO2↑、H2SO4+2NaOH=Na2SO4+2H2O、NaHCO3+NaOH=Na2CO3+H2O,能与其他三种物质均能反应的为硫酸,此物质是②。
(3)Al与稀硫酸反应生成Al2(SO4)3和H2,反应的化学方程式为2Al+3H2SO4=Al2(SO4)3+3H2↑,离子方程式为2Al+6H+=2Al3++3H2↑。在反应中Al元素的化合价由0价升至+3价,H元素的化合价由+1价降至0价,用双线桥表示为: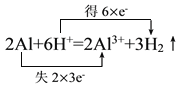 。
。

【题目】硝基苯是重要的精细化工原料,是医药和染料的中间体,还可做有机溶剂.制备硝基苯的过程如下: ①配制混酸:组装如图反应装置.取100 mL烧杯,用20 mL浓硫酸与浓硝酸18 mL配制混和酸,加入漏斗中.把18 mL苯加入三颈烧瓶中.
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀.
③在50﹣60℃下发生反应,直至反应结束.
④除去混和酸后,粗产品依次用蒸馏水和10%Na2CO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品.已知
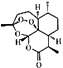
(i) ![]() +HNO3(浓)
+HNO3(浓) ![]()
![]() +H2O
+H2O 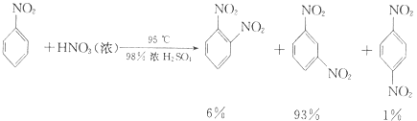
(ii)可能用到的有关数据列表如下
物质 | 熔点/℃ | 沸点/℃ | 密度(20℃)/gcm﹣3 | 溶解性 |
苯 | 5.5 | 80 | 0.88 | 微溶于水 |
硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
1,3﹣二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
浓硝酸 | 83 | 1.4 | 易溶于水 | |
浓硫酸 | 338 | 1.84 | 易溶于水 |
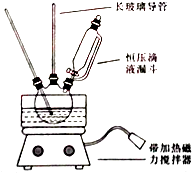
请回答下列问题:
(1)配置混酸应先在烧杯中先加入 .
(2)恒压滴液漏斗的优点是 .
(3)实验装置中长玻璃管可用代替(填仪器名称).
(4)反应结束后产品在液体的层(填“上”或者“下”),分离混酸和产品的操作方法为
(5)用10%Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净? .
(6)为了得到更纯净的硝基苯,还须先向液体中加入除去水,然后蒸馏,最终得到17.5g硝基苯,则硝基苯的产率为(保留两位有效数字).若加热后,发现未加沸石,应采取的操作是 .
【题目】滴定的方法有酸碱中和滴定、沉淀滴定、络合滴定等.沉淀滴定所用的指示剂本身就是一种沉淀剂.已知一些银盐的颜色和Ksp(20℃)如下,测定水体中氯化物的含量,常用标准硝酸银溶液进行滴定.
化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
Ksp | 1.8×10﹣10 | 5.0×10﹣13 | 8.3×10﹣17 | 2.0×10﹣48 | 1.8×10﹣10 |
滴定时,你认为该滴定适宜选用的指示剂是下列中的( )
A.KBr
B.KI
C.K2S
D.K2CrO4