题目内容
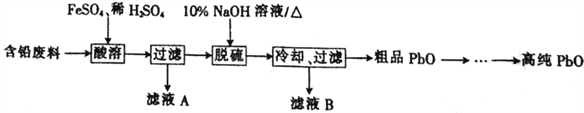
【题目】PbO(溶于酸,微溶于强碱溶液)在工业上用途广泛,可制作颜料铅白、杀虫剂等。某再生能源企业以含铅废料(主要含Pb、PbO、PbSO4和极少量的PbO2)和稀H2SO4为原料制备高纯PbO的工艺流程如下:
(1)含铅废料中的PbO2和PbSO4中,铅的化合价分别为____________、____________。
(2)酸溶过程中为了加快溶解速率,除了加入FeSO4作催化剂外,还可采取的措施有____________________(任写一种)。
(3)滤液A中含有的主要阳离子是____________________(填离子符号)。
(4)脱硫过程发生的主要反应的离子方程式为________________________________。
(5)冷却、过滤后对所得的固体进行洗涤操作,在实验室洗涤时,所用到的玻璃仪器有烧杯、_________和_________,检验沉淀是否洗涤干净的方法是________________________________。
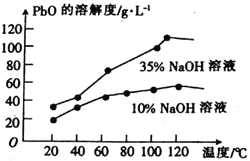
(6)PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)![]() NaHPbO2(aq)。PbO的溶解度曲线如图所示。结合该曲线,简述由粗品PbO得到高纯PbO的操作:_______________________________。
NaHPbO2(aq)。PbO的溶解度曲线如图所示。结合该曲线,简述由粗品PbO得到高纯PbO的操作:_______________________________。
【答案】 -4 -2 将含铅废料粉碎(或加热等其他合理答案) H+、Fe2+ PbSO4+2OH-![]() PbO+SO42- +H2O 玻璃棒 漏斗 取最后一次的洗涤液。做焰色反应实验,火焰不变黄色(或取最后一次的洗涤液。滴入BaCl2溶液,若不产生白色沉淀),则说明已洗涤干净 将粗PbO溶解在一定量35%NaOH溶液中,加热至110℃左右,充分溶解后,趁热过滤,将滤液冷却结晶,过滤、洗涤并干燥得到高纯PbO
PbO+SO42- +H2O 玻璃棒 漏斗 取最后一次的洗涤液。做焰色反应实验,火焰不变黄色(或取最后一次的洗涤液。滴入BaCl2溶液,若不产生白色沉淀),则说明已洗涤干净 将粗PbO溶解在一定量35%NaOH溶液中,加热至110℃左右,充分溶解后,趁热过滤,将滤液冷却结晶,过滤、洗涤并干燥得到高纯PbO
【解析】(1)含铅废料中的PbO2和PhSO4中,铅的化合价分别为+4、 +2;(2)酸溶过程中为了加快溶解速率,除了加入FeSO4作催化剂外,还可采取的措施有将含铅废料粉碎、适当升高温度、适当增大酸的浓度等;(3) 含铅废料中加入硫酸亚铁和硫酸溶解,生成硫酸铅为滤渣,滤液A中含有过量的硫酸和硫酸亚铁,故主要阳离子是H+、Fe2+;(4)脱硫过程发生是将硫酸铅转化为PbO,主要反应的离子方程式为PbSO4+2OH-![]() PbO+SO42-+H2O;(5)冷却、过滤后对所得的固体进行洗涤操作,在实验室洗涤时,所用到的玻璃仪器有烧杯、玻璃棒、漏斗,检验沉淀是否洗条干净的方法是取最后一次的洗涤液,做焰色反应实验,火焰不变黄色(或取最后一次白洗涤液.滴入BaCl2溶液,若不产生白色沉淀),则说明已洗涤干净;(6)PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)
PbO+SO42-+H2O;(5)冷却、过滤后对所得的固体进行洗涤操作,在实验室洗涤时,所用到的玻璃仪器有烧杯、玻璃棒、漏斗,检验沉淀是否洗条干净的方法是取最后一次的洗涤液,做焰色反应实验,火焰不变黄色(或取最后一次白洗涤液.滴入BaCl2溶液,若不产生白色沉淀),则说明已洗涤干净;(6)PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)![]() NaHPbO2(aq)PbO的溶解度曲线如图所示。结合该曲线,简述由粗品PbO得到高纯PbO的操作: 将粗PbO溶解在一定量35%NaOH溶液中,加热至110℃左右,充分溶解后,趁热过滤,将溶液冷却结晶,过滤、洗涤并干燥得到高纯PbO。
NaHPbO2(aq)PbO的溶解度曲线如图所示。结合该曲线,简述由粗品PbO得到高纯PbO的操作: 将粗PbO溶解在一定量35%NaOH溶液中,加热至110℃左右,充分溶解后,趁热过滤,将溶液冷却结晶,过滤、洗涤并干燥得到高纯PbO。

 阅读快车系列答案
阅读快车系列答案【题目】铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁.“速力菲”是市场上一种常见的补铁药品,其说明书部分内容摘录如下: 【规格】每片含琥珀酸亚铁0.1g
【适应症】用于缺铁性贫血症,预防及治疗用.
【贮藏】避光、密封、在干燥处保存.
【药物相互作用】与维生素C同服,可增加本品吸收;该药片在水和乙醇中溶解度不大
该药品中Fe2+会缓慢氧化.国家规定该药物中Fe2+的氧化率(已经被氧化Fe2+的质量与Fe2+总质量的比值)超过10.00% 即不能再服用.
(1)实验室可采用H2SO4酸化的KMnO4溶液,对“速力菲”中的Fe2+进行滴定(假设药品中其他成份不与KMnO4反应).滴定过程发生如下反应,请补充完整: Fe2++MnO4﹣+=Mn2+++ .
(2)实验前,称量含铁元素质量分数为20.00%的“速力菲”20.0g,将其全部溶于稀H2SO4中,配制成250ml溶液,配制时图1下列仪器肯定不需要的是 . (填名称)
(3)取配制好的溶液20.00ml于锥形瓶中,用0.1000mol/L﹣1的KMnO4溶液滴定,某同学设计了图2滴定方式(夹持部分略去),最合理的是(填字母序号);若滴定过程中,锥形瓶中待测液飞溅出来,则测出的Fe2+的氧化率(填偏高、偏低或不变).
(4)三次操作读数如下:
序号 | V初 | V末 | V标 |
① | 0.10mL | 9.71mL | 9.61mL |
② | 1.50mL | 11.09mL | 9.59mL |
③ | 0.50mL | 11.10mL | 11.60mL |
计算该“速力菲”补铁药品Fe2+的氧化率为%.

