题目内容
【题目】下列有关实验叙述正确的是( )
A.将过量硼酸(H3BO3)溶液加入Na2CO3溶液中,无明显现象,但发生了反应
B.根据密度的不同,用加水后再分液的方法可将苯和四氯化碳分离
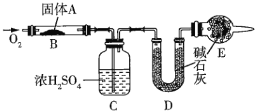
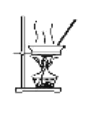
C.用如图装置蒸干溶液,可制得无水MnCl2固体
D.冷却Cu与浓硫酸反应后的液体,向其中加入水以观察CuSO4溶液的颜色
【答案】A
【解析】
A. 硼酸的酸性强于碳酸氢根,弱与碳酸,故将过量硼酸(H3BO3)溶液加入Na2CO3溶液中可反应生成碳酸氢钠,但无明显现象,故A正确;
B.苯和四氯化碳可以互溶,且都不溶于水,不能用水分离,故B错误;
C. MnCl2溶液中存在锰离子的水解,水解吸热,因此不能直接加热蒸发氯化锰溶液制MnCl2固体,应该在HCl的气氛中进行,故C错误;
D.反应后的液体残留大量硫酸,应将生成物加到水中,观察CuSO4溶液的颜色,试剂顺序颠倒,故D错误;
故答案为A。

练习册系列答案
相关题目
【题目】下表是![]() 时某些盐的浓度积常数和弱酸的电离平衡常数,下列说法正确的是
时某些盐的浓度积常数和弱酸的电离平衡常数,下列说法正确的是![]()
化学式 | AgCl |
|
| HClO |
|
Ksp或Ka |
|
|
|
|
|
A.相同浓度![]() 和NaClO的混合液中,各离子浓度的大小关系是
和NaClO的混合液中,各离子浓度的大小关系是![]()
B.向![]() 溶液中滴加NaOH溶液至
溶液中滴加NaOH溶液至![]() :
:![]() :9,此时溶液
:9,此时溶液![]()
C.碳酸钠溶液中滴加少量氯水的离子方程式为![]()
D.向浓度均为![]() 的KCl和
的KCl和![]() 混合液中滴加
混合液中滴加![]() 的
的![]() 溶液,
溶液,![]() 先形成沉淀.
先形成沉淀.